உங்களுக்குத் தெரியுமா? மனிதர்களின் செயல்முறை கண்டுபிடிக்கும்yttriumதிருப்பங்கள் மற்றும் சவால்கள் நிறைந்தவை. 1787 ஆம் ஆண்டில், ஸ்வீடன் கார்ல் ஆக்செல் அர்ஹீனியஸ் தற்செயலாக தனது சொந்த ஊரான யெட்டர்பி கிராமத்திற்கு அருகிலுள்ள ஒரு குவாரியில் அடர்த்தியான மற்றும் கனமான கருப்பு தாதுவைக் கண்டுபிடித்து அதற்கு "ytterbite" என்று பெயரிட்டார். அதன்பிறகு, ஜோஹன் கடோலின், ஆண்டர்ஸ் குஸ்டாவ் எக்பெர்க், ப்ரீட்ரிக் வஹ்லர் மற்றும் பலர் உட்பட பல விஞ்ஞானிகள் இந்த தாது குறித்து ஆழமான ஆராய்ச்சி மேற்கொண்டனர்.
1794 ஆம் ஆண்டில், பின்னிஷ் வேதியியலாளர் ஜோஹன் கடோலின் ஒரு புதிய ஆக்சைடை Ytterbium தாதுவிலிருந்து பிரித்து அதற்கு yttrium என்று பெயரிட்டார். ஒரு அரிய பூமி உறுப்பை மனிதர்கள் தெளிவாகக் கண்டுபிடிப்பது இதுவே முதல் முறை. இருப்பினும், இந்த கண்டுபிடிப்பு உடனடியாக பரவலான கவனத்தை ஈர்க்கவில்லை.
காலப்போக்கில், விஞ்ஞானிகள் பிற அரிய பூமி கூறுகளைக் கண்டுபிடித்துள்ளனர். 1803 ஆம் ஆண்டில், ஜெர்மன் கிளாப்ரோத் மற்றும் ஸ்வீடிஸ் ஹிட்ஸிங்கர் மற்றும் பெர்செலியஸ் ஆகியோர் சீரியத்தைக் கண்டுபிடித்தனர். 1839 ஆம் ஆண்டில், ஸ்வீடன் மொசாண்டர் கண்டுபிடித்தார்லந்தனம். 1843 ஆம் ஆண்டில், அவர் எர்பியம் மற்றும் கண்டுபிடித்தார்டெர்பியம். இந்த கண்டுபிடிப்புகள் அடுத்தடுத்த அறிவியல் ஆராய்ச்சிக்கு ஒரு முக்கியமான அடித்தளத்தை வழங்கின.
19 ஆம் நூற்றாண்டின் இறுதி வரை விஞ்ஞானிகள் "Yttrium" என்ற உறுப்பை Yttrium Ore இலிருந்து வெற்றிகரமாக பிரித்தனர். 1885 ஆம் ஆண்டில், ஆஸ்திரிய வில்ஸ்பாக் நியோடைமியம் மற்றும் பிரசோடைமியம் ஆகியவற்றைக் கண்டுபிடித்தார். 1886 ஆம் ஆண்டில், போயிஸ்-ப ud ட்ரான் கண்டுபிடித்தார்டிஸ்ப்ரோசியம். இந்த கண்டுபிடிப்புகள் அரிய பூமி கூறுகளின் பெரிய குடும்பத்தை மேலும் வளப்படுத்தின.
Yttrium கண்டுபிடிக்கப்பட்ட ஒரு நூற்றாண்டுக்கும் மேலாக, தொழில்நுட்ப நிலைமைகளின் வரம்புகள் காரணமாக, விஞ்ஞானிகள் இந்த உறுப்பை சுத்திகரிக்க முடியவில்லை, இது சில கல்வி மோதல்களையும் பிழைகளையும் ஏற்படுத்தியுள்ளது. இருப்பினும், இது விஞ்ஞானிகளை Yttrium படிப்பதற்கான உற்சாகத்திலிருந்து தடுக்கவில்லை.
20 ஆம் நூற்றாண்டின் முற்பகுதியில், அறிவியல் மற்றும் தொழில்நுட்பத்தின் தொடர்ச்சியான முன்னேற்றத்துடன், விஞ்ஞானிகள் இறுதியாக அரிய பூமி கூறுகளை சுத்திகரிக்க முடிந்தது. 1901 ஆம் ஆண்டில், பிரெஞ்சுக்காரர் யூஜின் டி மார்சேய் கண்டுபிடித்தார்யூரோபியம். 1907-1908 ஆம் ஆண்டில், ஆஸ்திரிய வில்ஸ்பாக் மற்றும் பிரெஞ்சுக்காரர் அர்பெய்ன் ஆகியோர் சுயாதீனமாக லுடேடியத்தை கண்டுபிடித்தனர். இந்த கண்டுபிடிப்புகள் அடுத்தடுத்த அறிவியல் ஆராய்ச்சிக்கு ஒரு முக்கியமான அடித்தளத்தை வழங்கின.
நவீன அறிவியல் மற்றும் தொழில்நுட்பத்தில், Yttrium இன் பயன்பாடு மேலும் மேலும் விரிவாகி வருகிறது. அறிவியல் மற்றும் தொழில்நுட்பத்தின் தொடர்ச்சியான முன்னேற்றத்துடன், Yttrium இன் நமது புரிதலும் பயன்பாடும் மேலும் மேலும் ஆழமாக மாறும்.
Yttrium உறுப்பின் பயன்பாட்டு புலங்கள்
1.ஆப்டிகல் கண்ணாடி மற்றும் மட்பாண்டங்கள்:ஆப்டிகல் கண்ணாடி மற்றும் மட்பாண்டங்கள் உற்பத்தியில் Yttrium பரவலாகப் பயன்படுத்தப்படுகிறது, முக்கியமாக வெளிப்படையான மட்பாண்டங்கள் மற்றும் ஆப்டிகல் கண்ணாடி உற்பத்தியில். அதன் கலவைகள் சிறந்த ஒளியியல் பண்புகளைக் கொண்டுள்ளன, மேலும் லேசர்கள், ஃபைபர்-ஆப்டிக் தகவல்தொடர்புகள் மற்றும் பிற உபகரணங்களின் கூறுகளை தயாரிக்க பயன்படுத்தலாம்.
2. பாஸ்பர்கள்:பாஸ்பர்களில் Yttrium கலவைகள் முக்கிய பங்கு வகிக்கின்றன மற்றும் பிரகாசமான ஒளிரும் தன்மையை வெளியிடலாம், எனவே அவை பெரும்பாலும் தொலைக்காட்சி திரைகள், மானிட்டர்கள் மற்றும் லைட்டிங் கருவிகளை தயாரிக்கப் பயன்படுகின்றன.Yttrium ஆக்சைடுமற்றும் பிற கலவைகள் பெரும்பாலும் ஒளியின் பிரகாசத்தையும் தெளிவையும் மேம்படுத்த ஒளிரும் பொருட்களாகப் பயன்படுத்தப்படுகின்றன.
3. அலாய் சேர்க்கைகள்: உலோக உலோகக் கலவைகளின் உற்பத்தியில், உலோகங்களின் இயந்திர பண்புகள் மற்றும் அரிப்பு எதிர்ப்பை மேம்படுத்த Yttrium பெரும்பாலும் ஒரு சேர்க்கையாகப் பயன்படுத்தப்படுகிறது.Yttrium கலவைகள்அதிக வலிமை எஃகு தயாரிக்க பெரும்பாலும் பயன்படுத்தப்படுகின்றனஅலுமினிய உலோகக் கலவைகள், அவற்றை அதிக வெப்ப-எதிர்ப்பு மற்றும் அரிப்பை எதிர்க்கும்.
4. வினையூக்கிகள்: சில வினையூக்கிகளில் Yttrium கலவைகள் முக்கிய பங்கு வகிக்கின்றன மற்றும் வேதியியல் எதிர்வினைகளின் வீதத்தை துரிதப்படுத்தலாம். தொழில்துறை உற்பத்தி செயல்முறைகளில் ஆட்டோமொபைல் வெளியேற்ற சுத்திகரிப்பு சாதனங்கள் மற்றும் வினையூக்கிகளை தயாரிக்க அவை பயன்படுத்தப்படுகின்றன, இது தீங்கு விளைவிக்கும் பொருட்களின் உமிழ்வைக் குறைக்க உதவுகிறது.
5. மருத்துவ இமேஜிங் தொழில்நுட்பம்: ரேடியோஃபார்மாசூட்டிகல்ஸ் லேபிளிங் மற்றும் அணு மருத்துவ இமேஜிங்கைக் கண்டறிதல் போன்ற கதிரியக்க ஐசோடோப்புகளைத் தயாரிக்க மருத்துவ இமேஜிங் தொழில்நுட்பத்தில் Yttrium ஐசோடோப்புகள் பயன்படுத்தப்படுகின்றன.
6. லேசர் தொழில்நுட்பம்:Yttrium அயன் லேசர்கள் என்பது பல்வேறு அறிவியல் ஆராய்ச்சி, லேசர் மருத்துவம் மற்றும் தொழில்துறை பயன்பாடுகளில் பயன்படுத்தப்படும் பொதுவான திட-நிலை லேசர் ஆகும். இந்த ஒளிக்கதிர்களின் உற்பத்திக்கு சில yttrium சேர்மங்களை ஆக்டிவேட்டர்களாகப் பயன்படுத்த வேண்டும்.Yttrium கூறுகள்நவீன அறிவியல் மற்றும் தொழில்நுட்பம் மற்றும் தொழில்துறையில் அவற்றின் சேர்மங்கள் முக்கிய பங்கு வகிக்கின்றன, இது ஒளியியல், பொருட்கள் அறிவியல் மற்றும் மருத்துவம் போன்ற பல துறைகளை உள்ளடக்கியது, மேலும் மனித சமுதாயத்தின் முன்னேற்றம் மற்றும் வளர்ச்சிக்கு சாதகமான பங்களிப்புகளைச் செய்துள்ளது.
Yttrium இன் இயற்பியல் பண்புகள்
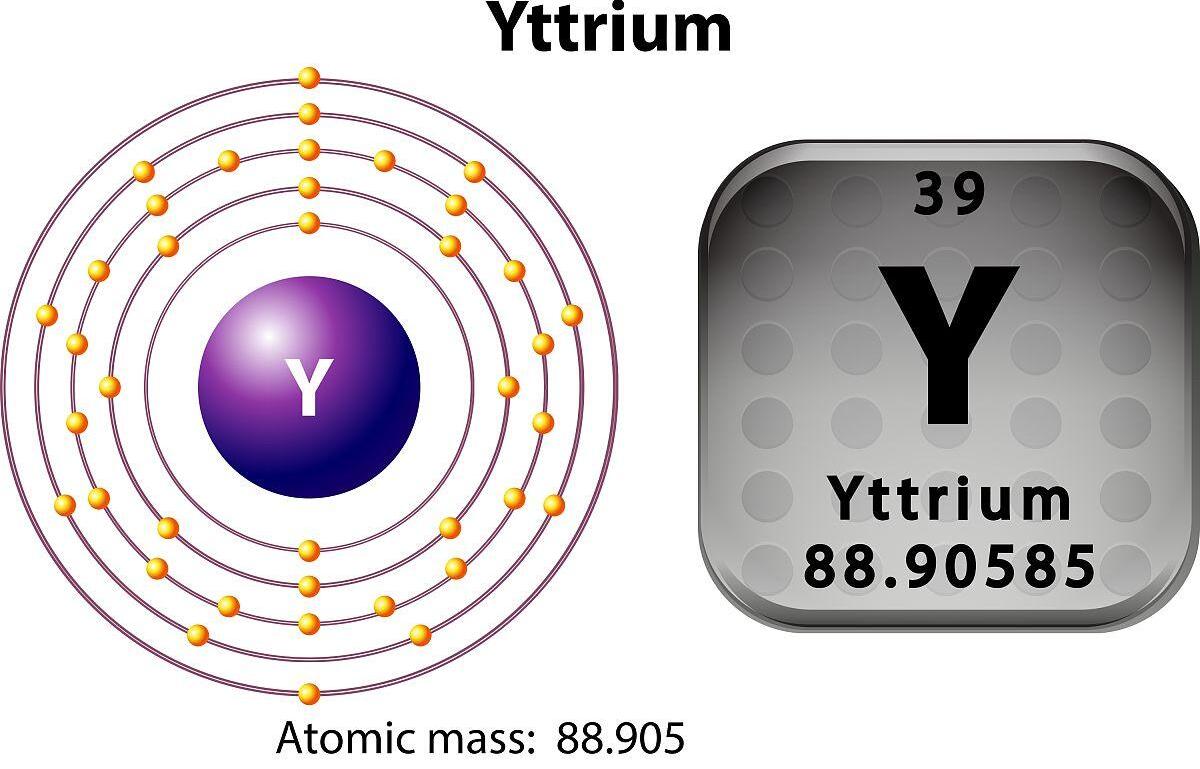
இன் அணு எண்yttrium39 மற்றும் அதன் வேதியியல் சின்னம் Y.
1. தோற்றம்:Yttrium ஒரு வெள்ளி-வெள்ளை உலோகம்.
2. அடர்த்தி:Yttrium இன் அடர்த்தி 4.47 கிராம்/செ.மீ 3 ஆகும், இது பூமியின் மேலோட்டத்தில் ஒப்பீட்டளவில் கனமான கூறுகளில் ஒன்றாகும்.
3. உருகும் புள்ளி:Yttrium இன் உருகும் புள்ளி 1522 டிகிரி செல்சியஸ் (2782 டிகிரி பாரன்ஹீட்) ஆகும், இது வெப்ப நிலைமைகளின் கீழ் ஒரு திடத்திலிருந்து ஒரு திரவத்திற்கு yttrium மாறும் வெப்பநிலையைக் குறிக்கிறது.
4. கொதிநிலை:Yttrium இன் கொதிநிலை 3336 டிகிரி செல்சியஸ் (6037 டிகிரி பாரன்ஹீட்) ஆகும், இது வெப்ப நிலைமைகளின் கீழ் ஒரு திரவத்திலிருந்து ஒரு வாயுவாக yttrium மாறும் வெப்பநிலையைக் குறிக்கிறது.
5. கட்டம்:அறை வெப்பநிலையில், Yttrium ஒரு திட நிலையில் உள்ளது.
6. கடத்துத்திறன்:Yttrium அதிக கடத்துத்திறன் கொண்ட மின்சாரத்தின் ஒரு நல்ல கடத்துக்காரர், எனவே இது மின்னணு சாதன உற்பத்தி மற்றும் சுற்று தொழில்நுட்பத்தில் சில பயன்பாடுகளைக் கொண்டுள்ளது.
7. காந்தவியல்:Yttrium என்பது அறை வெப்பநிலையில் ஒரு பரம காந்த பொருள் ஆகும், அதாவது காந்தப்புலங்களுக்கு வெளிப்படையான காந்த பதில் இல்லை.
8. படிக அமைப்பு: Yttrium ஒரு அறுகோண நெருக்கமான நிரம்பிய படிக கட்டமைப்பில் உள்ளது.
9. அணு தொகுதி:Yttrium இன் அணு அளவு ஒரு மோலுக்கு 19.8 கன சென்டிமீட்டர் ஆகும், இது Yttrium அணுக்களின் ஒரு மோலால் ஆக்கிரமிக்கப்பட்ட அளவைக் குறிக்கிறது.
Yttrium என்பது ஒப்பீட்டளவில் அதிக அடர்த்தி மற்றும் உருகும் புள்ளியைக் கொண்ட ஒரு உலோக உறுப்பு ஆகும், மேலும் நல்ல கடத்துத்திறனைக் கொண்டுள்ளது, எனவே இது மின்னணுவியல், பொருட்கள் அறிவியல் மற்றும் பிற துறைகளில் முக்கியமான பயன்பாடுகளைக் கொண்டுள்ளது. அதே நேரத்தில், Yttrium ஒப்பீட்டளவில் பொதுவான அரிதான உறுப்பு ஆகும், இது சில மேம்பட்ட தொழில்நுட்பங்கள் மற்றும் தொழில்துறை பயன்பாடுகளில் முக்கிய பங்கு வகிக்கிறது.
Yttrium இன் வேதியியல் பண்புகள்
1. வேதியியல் சின்னம் மற்றும் குழு: Yttrium இன் வேதியியல் சின்னம் y ஆகும், மேலும் இது கால அட்டவணையின் ஐந்தாவது காலகட்டத்தில் அமைந்துள்ளது, இது மூன்றாவது குழு, இது லாந்தனைடு கூறுகளுக்கு ஒத்ததாகும்.
2. மின்னணு அமைப்பு: Yttrium இன் மின்னணு அமைப்பு 1S² 2S² 2P⁶ 3S² 3p⁶ 3d⁰ 4S² 4p⁶ 4d⁰ 4f⁴ 5s² ஆகும். வெளிப்புற எலக்ட்ரான் அடுக்கில், Yttrium இரண்டு வேலன்ஸ் எலக்ட்ரான்களைக் கொண்டுள்ளது.
3. வேலன்ஸ் நிலை: Yttrium வழக்கமாக +3 இன் வேலன்ஸ் நிலையைக் காட்டுகிறது, இது மிகவும் பொதுவான வேலன்ஸ் நிலை, ஆனால் இது +2 மற்றும் +1 இன் வேலன்ஸ் நிலைகளையும் காட்டலாம்.
4. வினைத்திறன்: Yttrium என்பது ஒப்பீட்டளவில் நிலையான உலோகம், ஆனால் அது காற்றில் வெளிப்படும் போது படிப்படியாக ஆக்ஸிஜனேற்றும், மேற்பரப்பில் ஒரு ஆக்சைடு அடுக்கை உருவாக்குகிறது. இது Yttrium அதன் காந்தத்தை இழக்கச் செய்கிறது. Yttrium ஐப் பாதுகாக்க, இது பொதுவாக வறண்ட சூழலில் சேமிக்கப்படும்.
5. ஆக்சைடுகளுடனான எதிர்வினை: Yttrium ஆக்சைடுகளுடன் வினைபுரிந்து பல்வேறு சேர்மங்களை உருவாக்குகிறது, இதில் உட்படyttrium ஆக்சைடு(Y2o3). பாஸ்பர்கள் மற்றும் மட்பாண்டங்களை உருவாக்க Yttrium ஆக்சைடு பெரும்பாலும் பயன்படுத்தப்படுகிறது.
6. ** அமிலங்களுடன் எதிர்வினை **: yttrium வலுவான அமிலங்களுடன் வினைபுரிந்து தொடர்புடைய உப்புகளை உற்பத்தி செய்ய முடியும், அதாவதுyttrium குளோரைடு (Ycl3) அல்லதுyttrium சல்பேட் (Y2 (SO4) 3).
7. தண்ணீருடன் எதிர்வினை: Yttrium சாதாரண நிலைமைகளின் கீழ் நேரடியாக தண்ணீருடன் செயல்படாது, ஆனால் அதிக வெப்பநிலையில், இது நீர் நீராவியுடன் வினைபுரிந்து ஹைட்ரஜன் மற்றும் Yttrium ஆக்சைடை உற்பத்தி செய்யலாம்.
8. சல்பைடுகள் மற்றும் கார்பைடுகளுடன் எதிர்வினை: Yttrium சல்பைடுகள் மற்றும் கார்பைடுகளுடன் வினைபுரிந்து Yttrium Sulfide (YS) மற்றும் Yttrium கார்பைடு (YC2) போன்ற சேர்மங்களை உருவாக்கலாம். 9. ஐசோடோப்புகள்: Yttrium பல ஐசோடோப்புகளைக் கொண்டுள்ளது, அவற்றில் மிகவும் நிலையானது yttrium-89 (^89y) ஆகும், இது நீண்ட அரை ஆயுளைக் கொண்டுள்ளது மற்றும் அணு மருத்துவம் மற்றும் ஐசோடோப்பு லேபிளிங்கில் பயன்படுத்தப்படுகிறது.
Yttrium என்பது பல வேலன்ஸ் நிலைகளைக் கொண்ட ஒப்பீட்டளவில் நிலையான உலோக உறுப்பு மற்றும் சேர்மங்களை உருவாக்க மற்ற கூறுகளுடன் வினைபுரியும் திறன் ஆகும். இது ஒளியியல், பொருட்கள் அறிவியல், மருத்துவம் மற்றும் தொழில், குறிப்பாக பாஸ்பர்கள், பீங்கான் உற்பத்தி மற்றும் லேசர் தொழில்நுட்பத்தில் பரவலான பயன்பாடுகளைக் கொண்டுள்ளது.
Yttrium இன் உயிரியல் பண்புகள்
இன் உயிரியல் பண்புகள்yttriumவாழ்க்கை உயிரினங்களில் ஒப்பீட்டளவில் குறைவாகவே உள்ளன.
1. இருப்பு மற்றும் உட்கொள்ளல்: Yttrium வாழ்க்கைக்கு அவசியமான ஒரு உறுப்பு அல்ல என்றாலும், மண், பாறைகள் மற்றும் நீர் உள்ளிட்ட இயற்கையில் Yttrium இன் சுவடு அளவைக் காணலாம். பொதுவாக மண் மற்றும் தாவரங்களிலிருந்து, உணவுச் சங்கிலி வழியாக Yttrium இன் சுவடு அளவை உயிரினங்கள் உட்கொள்ளலாம்.
2. உயிர் கிடைக்கும் தன்மை: Yttrium இன் உயிர் கிடைக்கும் தன்மை ஒப்பீட்டளவில் குறைவாக உள்ளது, அதாவது உயிரினங்கள் பொதுவாக Yttrium ஐ திறம்பட உறிஞ்சி பயன்படுத்துவதில் சிரமம் உள்ளன. பெரும்பாலான yttrium சேர்மங்கள் உயிரினங்களில் எளிதில் உறிஞ்சப்படுவதில்லை, எனவே அவை வெளியேற்றப்படும்.
3. உயிரினங்களில் விநியோகம்: ஒரு உயிரினத்தில், Yttrium முக்கியமாக கல்லீரல், சிறுநீரகம், மண்ணீரல், நுரையீரல் மற்றும் எலும்புகள் போன்ற திசுக்களில் விநியோகிக்கப்படுகிறது. குறிப்பாக, எலும்புகளில் yttrium இன் அதிக செறிவுகள் உள்ளன.
4. வளர்சிதை மாற்றம் மற்றும் வெளியேற்றம்: மனித உடலில் Yttrium இன் வளர்சிதை மாற்றம் ஒப்பீட்டளவில் குறைவாகவே உள்ளது, ஏனெனில் இது வழக்கமாக உயிரினத்தை வெளியேற்றுவதன் மூலம் விட்டுவிடுகிறது. அதில் பெரும்பாலானவை சிறுநீர் மூலம் வெளியேற்றப்படுகின்றன, மேலும் இது மலம் கழிக்கும் வடிவத்திலும் வெளியேற்றப்படலாம்.
5. நச்சுத்தன்மை: அதன் குறைந்த உயிர் கிடைக்கும் தன்மை காரணமாக, Yttrium பொதுவாக சாதாரண உயிரினங்களில் தீங்கு விளைவிக்கும் அளவிற்கு குவிப்பதில்லை. இருப்பினும், அதிக அளவிலான Yttrium வெளிப்பாடு உயிரினங்களில் தீங்கு விளைவிக்கும் விளைவுகளை ஏற்படுத்தக்கூடும், இது நச்சு விளைவுகளுக்கு வழிவகுக்கும். இந்த நிலைமை பொதுவாக அரிதாகவே நிகழ்கிறது, ஏனெனில் இயற்கையில் Yttrium செறிவுகள் பொதுவாக குறைவாகவே உள்ளன, மேலும் இது உயிரினங்களுக்கு பரவலாகப் பயன்படுத்தப்படவில்லை அல்லது வெளிப்படும். உயிரினங்களில் Yttrium இன் உயிரியல் பண்புகள் முக்கியமாக சுவடு அளவுகள், குறைந்த உயிர் கிடைக்கும் தன்மை மற்றும் வாழ்க்கைக்கு அவசியமான ஒரு உறுப்பு அல்ல. சாதாரண சூழ்நிலைகளில் இது உயிரினங்களில் வெளிப்படையான நச்சு விளைவுகளை ஏற்படுத்தவில்லை என்றாலும், அதிக அளவிலான Yttrium வெளிப்பாடு சுகாதார அபாயங்களை ஏற்படுத்தக்கூடும். எனவே, Yttrium இன் பாதுகாப்பு மற்றும் உயிரியல் விளைவுகளுக்கு அறிவியல் ஆராய்ச்சி மற்றும் கண்காணிப்பு இன்னும் முக்கியமானது.
இயற்கையில் yttrium இன் விநியோகம்
Yttrium என்பது ஒரு அரிய பூமி உறுப்பு ஆகும், இது இயற்கையில் பரவலாக விநியோகிக்கப்படுகிறது, இருப்பினும் இது தூய அடிப்படை வடிவத்தில் இல்லை.
1. பூமியின் மேலோட்டத்தில் நிகழ்வு: பூமியின் மேலோட்டத்தில் yttrium இன் மிகுதியானது ஒப்பீட்டளவில் குறைவாக உள்ளது, சராசரியாக சுமார் 33 மி.கி/கி.கி. இது Yttrium ஐ அரிய கூறுகளில் ஒன்றாகும்.
Yttrium முக்கியமாக தாதுக்கள் வடிவில் உள்ளது, பொதுவாக மற்ற அரிய பூமி கூறுகளுடன். சில பெரிய Yttrium தாதுக்கள் Yttrium iron Garnet (YIG) மற்றும் Yttrium oxalate (Y2 (C2O4) 3) ஆகியவை அடங்கும்.
2. புவியியல் விநியோகம்: உலகெங்கிலும் Yttrium வைப்புக்கள் விநியோகிக்கப்படுகின்றன, ஆனால் சில பகுதிகள் Yttrium இல் பணக்காரமாக இருக்கலாம். ஆஸ்திரேலியா, சீனா, அமெரிக்கா, ரஷ்யா, கனடா, இந்தியா, ஸ்காண்டிநேவியா போன்ற சில பெரிய Yttrium வைப்புகளை பின்வரும் பிராந்தியங்களில் காணலாம். 3. பிரித்தெடுத்தல் மற்றும் செயலாக்கம்: Yttrium தாது வெட்டப்பட்டவுடன், வேதியியல் செயலாக்கம் பொதுவாக Yttrium ஐ பிரித்தெடுக்கவும் பிரிக்கவும் தேவைப்படுகிறது. இது வழக்கமாக அதிக தூய்மை Yttrium ஐப் பெற அமில கசிவு மற்றும் வேதியியல் பிரிப்பு செயல்முறைகளை உள்ளடக்கியது.
Yttrium போன்ற அரிய பூமி கூறுகள் பொதுவாக தூய கூறுகளின் வடிவத்தில் இல்லை, ஆனால் பிற அரிய பூமி கூறுகளுடன் கலக்கப்படுகின்றன என்பதை கவனத்தில் கொள்ள வேண்டும். எனவே, அதிக தூய்மை Yttrium ஐ பிரித்தெடுப்பதற்கு சிக்கலான வேதியியல் செயலாக்கம் மற்றும் பிரிப்பு செயல்முறைகள் தேவை. கூடுதலாக, வழங்கல்அரிய பூமி கூறுகள்வரையறுக்கப்பட்டுள்ளது, எனவே அவற்றின் வள மேலாண்மை மற்றும் சுற்றுச்சூழல் நிலைத்தன்மையைக் கருத்தில் கொள்வதும் முக்கியம்.
சுரங்க, பிரித்தெடுத்தல் மற்றும் yttrium உறுப்பின் கரணம்
Yttrium என்பது ஒரு அரிய பூமி உறுப்பு ஆகும், இது பொதுவாக தூய yttrium வடிவத்தில் இல்லை, ஆனால் Yttrium தாது வடிவத்தில் இல்லை. பின்வருவது Yttrium உறுப்பின் சுரங்க மற்றும் சுத்திகரிப்பு செயல்முறைக்கு விரிவான அறிமுகம்:
1. Yttrium Ore இன் சுரங்க:
ஆய்வு: முதலாவதாக, புவியியலாளர்கள் மற்றும் சுரங்க பொறியியலாளர்கள் Yttrium ஐக் கொண்ட வைப்புகளைக் கண்டறிய ஆய்வுப் பணிகளை மேற்கொள்கின்றனர். இது பொதுவாக புவியியல் ஆய்வுகள், புவி இயற்பியல் ஆய்வு மற்றும் மாதிரி பகுப்பாய்வு ஆகியவற்றை உள்ளடக்கியது. சுரங்க: yttrium கொண்ட ஒரு வைப்பு கிடைத்தவுடன், தாது வெட்டப்படுகிறது. இந்த வைப்புகளில் பொதுவாக Yttrium இரும்பு கார்னெட் (YIG) அல்லது Yttrium ஆக்சலேட் (Y2 (C2O4) 3) போன்ற ஆக்சைடு தாதுக்கள் அடங்கும். தாது நொறுக்குதல்: சுரங்கத்திற்குப் பிறகு, தாது பொதுவாக அடுத்தடுத்த செயலாக்கத்திற்காக சிறிய துண்டுகளாக உடைக்கப்பட வேண்டும்.
2. Yttrium ஐ பிரித்தெடுத்தல்:வேதியியல் கசிவு: நொறுக்கப்பட்ட தாது வழக்கமாக ஒரு ஸ்மெல்ட்டருக்கு அனுப்பப்படுகிறது, அங்கு Yttrium ரசாயன கசிவு மூலம் பிரித்தெடுக்கப்படுகிறது. இந்த செயல்முறை பொதுவாக தாதுவிலிருந்து yttrium ஐ கரைக்க சல்பூரிக் அமிலம் போன்ற அமிலக் கசிவு தீர்வைப் பயன்படுத்துகிறது. பிரித்தல்: yttrium கரைந்தவுடன், இது வழக்கமாக மற்ற அரிய பூமி கூறுகள் மற்றும் அசுத்தங்களுடன் கலக்கப்படுகிறது. அதிக தூய்மையின் yttrium ஐ பிரித்தெடுக்க, ஒரு பிரிப்பு செயல்முறை தேவைப்படுகிறது, பொதுவாக கரைப்பான் பிரித்தெடுத்தல், அயன் பரிமாற்றம் அல்லது பிற வேதியியல் முறைகளைப் பயன்படுத்துகிறது. மழைப்பொழிவு: தூய்மையான yttrium சேர்மங்களை உருவாக்குவதற்கு பொருத்தமான வேதியியல் எதிர்வினைகள் மூலம் Yttrium பிற அரிய பூமி கூறுகளிலிருந்து பிரிக்கப்படுகிறது. உலர்த்துதல் மற்றும் கணக்கீடு: பெறப்பட்ட Yttrium கலவைகள் பொதுவாக தூய yttrium உலோகம் அல்லது சேர்மங்களைப் பெறுவதற்கு எஞ்சிய ஈரப்பதம் மற்றும் அசுத்தங்களை அகற்ற பொதுவாக உலர்த்தப்பட்டு கணக்கிடப்பட வேண்டும்.
Yttrium இன் கண்டறிதல் முறைகள்
Yttrium க்கான பொதுவான கண்டறிதல் முறைகள் முக்கியமாக அணு உறிஞ்சுதல் ஸ்பெக்ட்ரோஸ்கோபி (AAS), தூண்டலாக இணைந்த பிளாஸ்மா மாஸ் ஸ்பெக்ட்ரோமெட்ரி (ICP-MS), எக்ஸ்-ரே ஃப்ளோரசன்ஸ் ஸ்பெக்ட்ரோஸ்கோபி (எக்ஸ்ஆர்எஃப்) போன்றவை அடங்கும்.
1. அணு உறிஞ்சுதல் ஸ்பெக்ட்ரோஸ்கோபி (ஏஏஎஸ்):AAS என்பது பொதுவாக பயன்படுத்தப்படும் அளவு பகுப்பாய்வு முறையாகும், இது Yttrium உள்ளடக்கத்தை கரைசலில் தீர்மானிக்க ஏற்றது. மாதிரியில் உள்ள இலக்கு உறுப்பு ஒரு குறிப்பிட்ட அலைநீளத்தின் ஒளியை உறிஞ்சும் போது இந்த முறை உறிஞ்சுதல் நிகழ்வை அடிப்படையாகக் கொண்டது. முதலாவதாக, எரிவாயு எரிப்பு மற்றும் உயர் வெப்பநிலை உலர்த்துதல் போன்ற முன் சிகிச்சை படிகள் மூலம் மாதிரி அளவிடக்கூடிய வடிவமாக மாற்றப்படுகிறது. பின்னர், இலக்கு உறுப்பின் அலைநீளத்துடன் தொடர்புடைய ஒளி மாதிரியில் அனுப்பப்படுகிறது, மாதிரியால் உறிஞ்சப்படும் ஒளி தீவிரம் அளவிடப்படுகிறது, மேலும் மாதிரியில் உள்ள Yttrium உள்ளடக்கம் அறியப்பட்ட செறிவின் நிலையான Yttrium தீர்வுடன் ஒப்பிடுவதன் மூலம் கணக்கிடப்படுகிறது.
2. தூண்டலாக இணைந்த பிளாஸ்மா மாஸ் ஸ்பெக்ட்ரோமெட்ரி (ஐ.சி.பி-எம்.எஸ்):ஐ.சி.பி-எம்.எஸ் என்பது திரவ மற்றும் திட மாதிரிகளில் Yttrium உள்ளடக்கத்தை தீர்மானிக்க ஏற்றது. இந்த முறை மாதிரியை சார்ஜ் செய்யப்பட்ட துகள்களாக மாற்றுகிறது, பின்னர் வெகுஜன பகுப்பாய்விற்கு வெகுஜன நிறமாலை பயன்படுத்துகிறது. ஐ.சி.பி-எம்.எஸ் ஒரு பரந்த கண்டறிதல் வரம்பு மற்றும் உயர் தெளிவுத்திறனைக் கொண்டுள்ளது, மேலும் ஒரே நேரத்தில் பல உறுப்புகளின் உள்ளடக்கத்தை தீர்மானிக்க முடியும். Yttrium ஐக் கண்டறிவதற்கு, ICP-MS மிகக் குறைந்த கண்டறிதல் வரம்புகளையும் அதிக துல்லியத்தையும் வழங்க முடியும்.
3. எக்ஸ்ரே ஃப்ளோரசன்ஸ் ஸ்பெக்ட்ரோமெட்ரி (எக்ஸ்ஆர்எஃப்):எக்ஸ்ஆர்எஃப் என்பது திட மற்றும் திரவ மாதிரிகளில் Yttrium உள்ளடக்கத்தை நிர்ணயிப்பதற்கு ஏற்ற ஒரு அழிவில்லாத பகுப்பாய்வு முறையாகும். இந்த முறை எக்ஸ்-கதிர்களுடன் மாதிரியின் மேற்பரப்பை கதிர்வீச்சு செய்வதன் மூலமும், மாதிரியில் உள்ள ஃப்ளோரசன் ஸ்பெக்ட்ரமின் சிறப்பியல்பு உச்ச தீவிரத்தை அளவிடுவதன் மூலமும் உறுப்பு உள்ளடக்கத்தை தீர்மானிக்கிறது. எக்ஸ்ஆர்எஃப் வேகமான வேகம், எளிய செயல்பாடு மற்றும் ஒரே நேரத்தில் பல கூறுகளைத் தீர்மானிக்கும் திறனைக் கொண்டுள்ளது. இருப்பினும், குறைந்த உள்ளடக்க Yttrium இன் பகுப்பாய்வில் எக்ஸ்ஆர்எஃப் தலையிடக்கூடும், இதன் விளைவாக பெரிய பிழைகள் ஏற்படுகின்றன.
4. தூண்டலாக இணைந்த பிளாஸ்மா ஆப்டிகல் உமிழ்வு ஸ்பெக்ட்ரோமெட்ரி (ஐ.சி.பி-ஓஸ்):தூண்டக்கூடிய இணைந்த பிளாஸ்மா ஆப்டிகல் உமிழ்வு ஸ்பெக்ட்ரோமெட்ரி என்பது பல-உறுப்பு பகுப்பாய்வில் பரவலாகப் பயன்படுத்தப்படும் மிகவும் உணர்திறன் மற்றும் தேர்ந்தெடுக்கப்பட்ட பகுப்பாய்வு முறையாகும். இது மாதிரியை அணுக்க்கிறது மற்றும் குறிப்பிட்ட அலைநீளம் மற்றும் தீவிரத்தை அளவிட ஒரு பிளாஸ்மாவை உருவாக்குகிறதுf yttriumஸ்பெக்ட்ரோமீட்டரில் உமிழ்வு. மேற்கண்ட முறைகளுக்கு மேலதிகமாக, எலக்ட்ரோ கெமிக்கல் முறை, ஸ்பெக்ட்ரோஃபோட்டோமெட்ரி போன்றவை உட்பட Yttrium கண்டறிதலுக்கான பொதுவாகப் பயன்படுத்தப்படும் பிற முறைகள் உள்ளன. பொருத்தமான கண்டறிதல் முறையைத் தேர்ந்தெடுப்பது மாதிரி பண்புகள், தேவையான அளவீட்டு வரம்பு மற்றும் கண்டறிதல் துல்லியம் போன்ற காரணிகளைப் பொறுத்தது, மேலும் அளவீட்டு முடிவுகளின் துல்லியம் மற்றும் நம்பகத்தன்மையை உறுதிப்படுத்த அளவுத்திருத்த தரநிலைகள் பெரும்பாலும் தேவைப்படுகின்றன.
Yttrium அணு உறிஞ்சுதல் முறையின் குறிப்பிட்ட பயன்பாடு
உறுப்பு அளவீட்டில், தூண்டக்கூடிய இணைந்த பிளாஸ்மா மாஸ் ஸ்பெக்ட்ரோமெட்ரி (ஐ.சி.பி-எம்.எஸ்) என்பது மிகவும் உணர்திறன் மற்றும் பல-உறுப்பு பகுப்பாய்வு நுட்பமாகும், இது பெரும்பாலும் Yttrium உள்ளிட்ட உறுப்புகளின் செறிவைத் தீர்மானிக்கப் பயன்படுகிறது. ஐ.சி.பி-எம்.எஸ்ஸில் Yttrium ஐ சோதிப்பதற்கான விரிவான செயல்முறை பின்வருமாறு:
1. மாதிரி தயாரிப்பு:
மாதிரி வழக்கமாக ஐ.சி.பி-எம்.எஸ் பகுப்பாய்விற்கான ஒரு திரவ வடிவத்தில் கலைக்கப்பட வேண்டும் அல்லது சிதறடிக்கப்பட வேண்டும். வேதியியல் கலைப்பு, வெப்பமூட்டும் செரிமானம் அல்லது பிற பொருத்தமான தயாரிப்பு முறைகள் மூலம் இதைச் செய்யலாம்.
மாதிரியைத் தயாரிப்பதற்கு எந்தவொரு வெளிப்புற கூறுகளாலும் மாசுபடுவதைத் தடுக்க மிகவும் சுத்தமான நிலைமைகள் தேவைப்படுகின்றன. மாதிரி மாசுபடுவதைத் தவிர்க்க ஆய்வகம் தேவையான நடவடிக்கைகளை எடுக்க வேண்டும்.
2. ஐ.சி.பி தலைமுறை:
மூடிய குவார்ட்ஸ் பிளாஸ்மா டார்ச்சில் ஆர்கான் அல்லது ஆர்கான்-ஆக்ஸிஜன் கலப்பு வாயுவை அறிமுகப்படுத்துவதன் மூலம் ஐ.சி.பி உருவாக்கப்படுகிறது. உயர் அதிர்வெண் தூண்டல் இணைப்பு ஒரு தீவிரமான பிளாஸ்மா சுடரை உருவாக்குகிறது, இது பகுப்பாய்வின் தொடக்க புள்ளியாகும்.
பிளாஸ்மாவின் வெப்பநிலை சுமார் 8000 முதல் 10000 டிகிரி செல்சியஸ் ஆகும், இது மாதிரியில் உள்ள கூறுகளை அயனி நிலையாக மாற்றும் அளவுக்கு அதிகமாக உள்ளது.
3. அயனியாக்கம் மற்றும் பிரிப்பு:மாதிரி பிளாஸ்மாவுக்குள் நுழைந்ததும், அதில் உள்ள கூறுகள் அயனியாக்கம் செய்யப்படுகின்றன. இதன் பொருள் அணுக்கள் ஒன்று அல்லது அதற்கு மேற்பட்ட எலக்ட்ரான்களை இழந்து, சார்ஜ் செய்யப்பட்ட அயனிகளை உருவாக்குகின்றன. ஐ.சி.பி-எம்.எஸ் வெவ்வேறு உறுப்புகளின் அயனிகளைப் பிரிக்க ஒரு வெகுஜன ஸ்பெக்ட்ரோமீட்டரைப் பயன்படுத்துகிறது, பொதுவாக வெகுஜன-கட்டண விகிதம் (எம்/இசட்) மூலம். இது வெவ்வேறு கூறுகளின் அயனிகளை பிரித்து பின்னர் பகுப்பாய்வு செய்ய அனுமதிக்கிறது.
4. வெகுஜன நிறமாலை:பிரிக்கப்பட்ட அயனிகள் ஒரு வெகுஜன நிறமாலை, பொதுவாக ஒரு நான்கு மடங்கு வெகுஜன நிறமாலை அல்லது காந்த ஸ்கேனிங் மாஸ் ஸ்பெக்ட்ரோமீட்டருக்குள் நுழைகின்றன. மாஸ் ஸ்பெக்ட்ரோமீட்டரில், வெவ்வேறு உறுப்புகளின் அயனிகள் அவற்றின் வெகுஜன-கட்டண விகிதத்திற்கு ஏற்ப பிரிக்கப்பட்டு கண்டறியப்படுகின்றன. இது ஒவ்வொரு உறுப்பின் இருப்பையும் செறிவையும் தீர்மானிக்க அனுமதிக்கிறது. தூண்டக்கூடிய இணைந்த பிளாஸ்மா மாஸ் ஸ்பெக்ட்ரோமெட்ரியின் நன்மைகளில் ஒன்று அதன் உயர் தெளிவுத்திறன் கொண்டது, இது ஒரே நேரத்தில் பல கூறுகளைக் கண்டறிய உதவுகிறது.
5. தரவு செயலாக்கம்:ICP-MS ஆல் உருவாக்கப்படும் தரவு வழக்கமாக மாதிரியில் உள்ள உறுப்புகளின் செறிவை தீர்மானிக்க செயலாக்கப்பட்டு பகுப்பாய்வு செய்யப்பட வேண்டும். கண்டறிதல் சமிக்ஞையை அறியப்பட்ட செறிவுகளின் தரங்களுடன் ஒப்பிடுவதும், அளவுத்திருத்தம் மற்றும் திருத்தம் செய்வதும் இதில் அடங்கும்.
6. முடிவு அறிக்கை:இறுதி முடிவு உறுப்பின் செறிவு அல்லது வெகுஜன சதவீதமாக வழங்கப்படுகிறது. இந்த முடிவுகளை பூமி அறிவியல், சுற்றுச்சூழல் பகுப்பாய்வு, உணவு சோதனை, மருத்துவ ஆராய்ச்சி போன்ற பல்வேறு பயன்பாடுகளில் பயன்படுத்தலாம்.
ஐ.சி.பி-எம்.எஸ் என்பது Yttrium உட்பட பல உறுப்பு பகுப்பாய்வுகளுக்கு ஏற்ற மிகவும் துல்லியமான மற்றும் உணர்திறன் நுட்பமாகும். இருப்பினும், இதற்கு சிக்கலான கருவி மற்றும் நிபுணத்துவம் தேவைப்படுகிறது, எனவே இது வழக்கமாக ஒரு ஆய்வகம் அல்லது தொழில்முறை பகுப்பாய்வு மையத்தில் செய்யப்படுகிறது. உண்மையான வேலையில், தளத்தின் குறிப்பிட்ட தேவைகளுக்கு ஏற்ப பொருத்தமான அளவீட்டு முறையைத் தேர்ந்தெடுப்பது அவசியம். இந்த முறைகள் ஆய்வகங்கள் மற்றும் தொழில்களில் ytterbium ஐ பகுப்பாய்வு செய்வதிலும் கண்டறிதலிலும் பரவலாகப் பயன்படுத்தப்படுகின்றன.
மேற்கூறியவற்றை சுருக்கமாகக் கொண்ட பிறகு, Yttrium என்பது தனித்துவமான உடல் மற்றும் வேதியியல் பண்புகளைக் கொண்ட மிகவும் சுவாரஸ்யமான வேதியியல் உறுப்பு என்று நாம் முடிவு செய்யலாம், இது அறிவியல் ஆராய்ச்சி மற்றும் பயன்பாட்டுத் துறைகளில் மிகவும் முக்கியத்துவம் வாய்ந்தது. அதைப் பற்றிய நமது புரிதலில் நாங்கள் சில முன்னேற்றங்களைச் செய்திருந்தாலும், மேலும் ஆராய்ச்சி மற்றும் ஆய்வு தேவைப்படும் பல கேள்விகள் இன்னும் உள்ளன. எங்கள் அறிமுகம் இந்த கவர்ச்சிகரமான கூறுகளை நன்கு புரிந்துகொள்ளவும், விஞ்ஞானத்தின் மீதான அனைவரின் அன்பையும், ஆய்வில் ஆர்வத்தையும் ஊக்குவிக்கவும் வாசகர்களுக்கு உதவும் என்று நம்புகிறேன்.
மேலும் தகவலுக்கு plsஎங்களைத் தொடர்பு கொள்ளுங்கள்கீழே:
தொலைபேசி & வாட்ஸ்: 008613524231522
Email:Sales@shxlchem.com
இடுகை நேரம்: நவம்பர் -28-2024