Het jy geweet? Die proses van mense wat ontdekyttriumwas vol kinkels en uitdagings. In 1787 ontdek die Swede Karl Axel Arrhenius per ongeluk 'n digte en swaar swart erts in 'n steengroef naby sy tuisdorp Ytterby Village en noem dit 'Ytterbite'. Daarna het baie wetenskaplikes, waaronder Johan Gadolin, Anders Gustav Ekberg, Friedrich Wöhler en andere diepgaande navorsing oor hierdie erts gedoen.
In 1794 het die Finse chemikus Johan Gadolin 'n nuwe oksied van ytterbium erts suksesvol geskei en dit yttrium genoem. Dit was die eerste keer dat die mens duidelik 'n seldsame aarde -element ontdek het. Hierdie ontdekking het egter nie onmiddellik wydverspreide aandag getrek nie.
Met verloop van tyd het wetenskaplikes ander seldsame aardelemente ontdek. In 1803 het die Duitse Klaproth en die Swede Hitzinger en Berzelius Cerium ontdek. In 1839 ontdek die Swede Mosanderlanthanum. In 1843 ontdek hy erbium enterbium. Hierdie ontdekkings het 'n belangrike basis gelewer vir daaropvolgende wetenskaplike navorsing.
Dit was eers aan die einde van die 19de eeu dat wetenskaplikes die element "yttrium" van yttrium erts suksesvol geskei het. In 1885 ontdek die Oostenrykse Wilsbach neodymium en praseodymium. In 1886 ontdek Bois-Baudrandisprosium. Hierdie ontdekkings het die groot familie van seldsame aardelemente verder verryk.
Vir meer as 'n eeu na die ontdekking van Yttrium, weens die beperkinge van tegniese toestande, kon wetenskaplikes nie hierdie element suiwer nie, wat ook akademiese geskille en foute veroorsaak het. Dit het egter nie die wetenskaplikes van hul entoesiasme vir die bestudering van Yttrium verhinder nie.
In die vroeë 20ste eeu, met die voortdurende bevordering van wetenskap en tegnologie, het wetenskaplikes uiteindelik seldsame aardelemente begin suiwer. In 1901 ontdek die Fransman Eugene de MarseilleEuropium. In 1907-1908 het die Oostenrykse Wilsbach en Fransman Urbain onafhanklik Lutetium ontdek. Hierdie ontdekkings het 'n belangrike basis gelewer vir daaropvolgende wetenskaplike navorsing.
In moderne wetenskap en tegnologie word die toepassing van Yttrium al hoe meer uitgebreid. Met die voortdurende bevordering van wetenskap en tegnologie, sal ons begrip en toepassing van Yttrium meer en meer diepgaande word.
Toepassingsvelde van yttrium -element
1.Optiese glas en keramiek:Yttrium word wyd gebruik in die vervaardiging van optiese glas en keramiek, hoofsaaklik in die vervaardiging van deursigtige keramiek en optiese glas. Die verbindings het uitstekende optiese eienskappe en kan gebruik word om komponente van lasers, veseloptiese kommunikasie en ander toerusting te vervaardig.
2. Fosfore:Yttriumverbindings speel 'n belangrike rol in fosfore en kan helder fluoressensie uitstraal, en dit word dikwels gebruik om TV -skerms, monitors en beligtingstoerusting te vervaardig.Yttriumoksieden ander verbindings word dikwels as luminescerende materiale gebruik om die helderheid en helderheid van lig te verbeter.
3. Allooi -bymiddels: In die produksie van metaallegerings word yttrium dikwels gebruik as toevoeging om die meganiese eienskappe en korrosie -weerstand van metale te verbeter.Yttrium legeringsword dikwels gebruik om staal met 'n hoë sterkte enaluminiumlegeringswat hulle meer hittebestand en korrosiebestand maak.
4. Katalisators: Yttriumverbindings speel 'n belangrike rol in sommige katalisators en kan die tempo van chemiese reaksies versnel. Dit word gebruik om motoruitlaat -suiweringsapparate en katalisators in industriële produksieprosesse te vervaardig, wat help om die emissie van skadelike stowwe te verminder.
5. Mediese beeldvormingstegnologie: Yttrium -isotope word in mediese beeldvormingstegnologie gebruik om radioaktiewe isotope voor te berei, soos vir die etikettering van radiofarmaseutiese produkte en die diagnosering van kernmediese beeldvorming.
6. Laser -tegnologie:Yttrium-ion-lasers is 'n gemeenskaplike laser met vaste toestand wat in verskillende wetenskaplike navorsing, lasergeneeskunde en industriële toepassings gebruik word. Die vervaardiging van hierdie lasers benodig die gebruik van sekere yttriumverbindings as aktivators.YttriumelementeEn hul verbindings speel 'n belangrike rol in die moderne wetenskap en tegnologie en nywerheid, waarby baie velde soos optika, materiale wetenskap en medisyne betrokke is, en positiewe bydraes gelewer het tot die vooruitgang en ontwikkeling van die menslike samelewing.
Fisiese eienskappe van yttrium
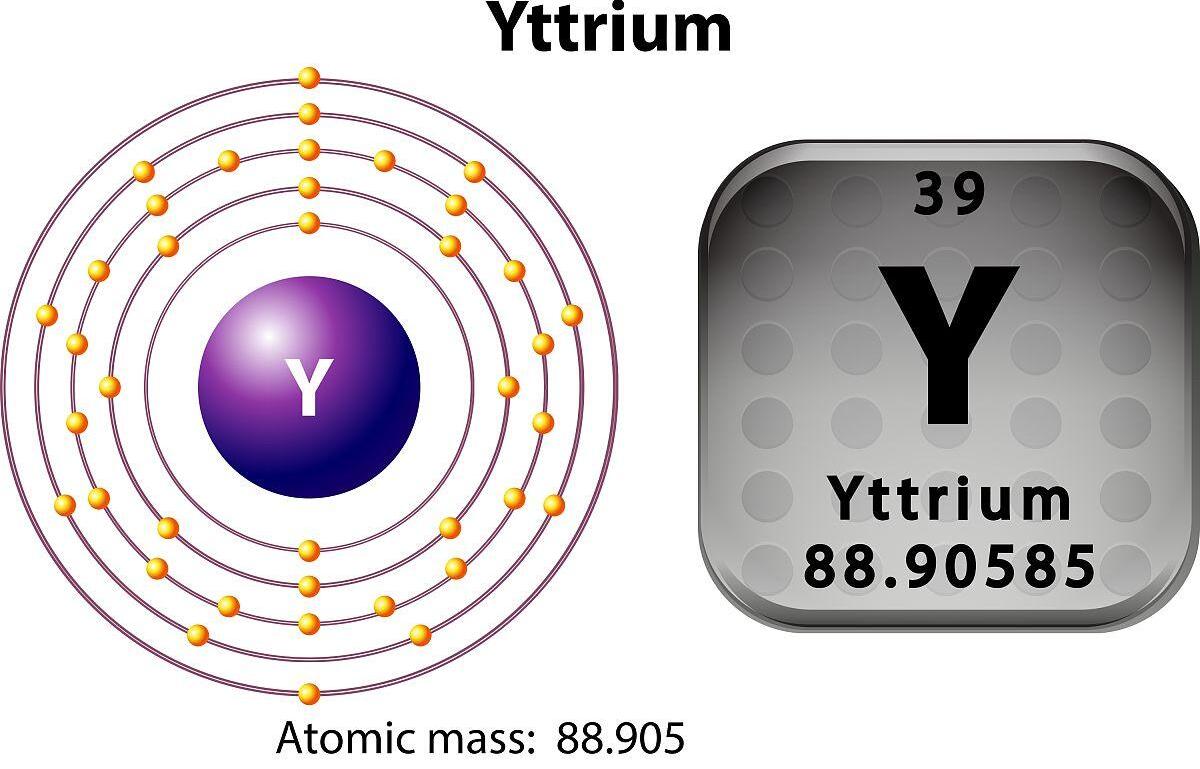
Die atoomgetal vanyttriumis 39 en die chemiese simbool daarvan is Y.
1. voorkoms:Yttrium is 'n silwerwit metaal.
2. Digtheid:Die digtheid van Yttrium is 4,47 g/cm3, wat dit een van die relatiewe swaar elemente in die aardkors maak.
3. Smeltpunt:Die smeltpunt van Yttrium is 1522 grade Celsius (2782 grade Fahrenheit), wat verwys na die temperatuur waarteen yttrium verander van 'n vaste stof na 'n vloeistof onder termiese toestande.
4. Kookpunt:Die kookpunt van Yttrium is 3336 grade Celsius (6037 grade Fahrenheit), wat verwys na die temperatuur waarteen yttrium verander van 'n vloeistof na 'n gas onder termiese toestande.
5. Fase:By kamertemperatuur is Yttrium in 'n vaste toestand.
6. Geleidingsvermoë:Yttrium is 'n goeie geleier van elektrisiteit met 'n hoë geleidingsvermoë, dus het dit sekere toepassings in die vervaardiging van elektroniese toestelle en kringtegnologie.
7. Magnetisme:Yttrium is 'n paramagnetiese materiaal by kamertemperatuur, wat beteken dat dit nie duidelike magnetiese reaksie op magnetiese velde het nie.
8. kristalstruktuur: Yttrium bestaan in 'n seskantige kristalstruktuur wat nou gepak is.
9. Atoomvolume:Die atoomvolume van yttrium is 19,8 kubieke sentimeter per mol, wat verwys na die volume wat deur een mol yttriumatome beset word.
Yttrium is 'n metaalelement met 'n relatiewe hoë digtheid en smeltpunt en het goeie geleidingsvermoë, dus het dit belangrike toepassings in elektronika, materiale wetenskap en ander velde. Terselfdertyd is Yttrium ook 'n relatiewe algemene seldsame element, wat 'n belangrike rol speel in sommige gevorderde tegnologieë en industriële toepassings.
Chemiese eienskappe van yttrium
1. Chemiese simbool en groep: Die chemiese simbool van yttrium is y, en is geleë in die vyfde periode van die periodieke tabel, die derde groep, wat soortgelyk is aan die lantaniedelemente.
2. Elektroniese struktuur: Die elektroniese struktuur van Yttrium is 1S² 2S² 2P⁶ 3S² 3P⁶ 3D¹⁰ 4S² 4P⁶ 4D¹⁰ 4F¹⁴ 5S². In die buitenste elektronlaag het Yttrium twee valenselektrone.
3. Valensietoestand: Yttrium toon gewoonlik 'n valensietoestand van +3, wat die algemeenste valensietoestand is, maar dit kan ook valensietoestande van +2 en +1 toon.
4. Reaktiwiteit: Yttrium is 'n relatiewe stabiele metaal, maar dit sal geleidelik oksideer as dit aan lug blootgestel word, wat 'n oksiedlaag op die oppervlak vorm. Dit veroorsaak dat Yttrium sy glans verloor. Om Yttrium te beskerm, word dit gewoonlik in 'n droë omgewing geberg.
5. reaksie met oksiede: yttrium reageer met oksiede om verskillende verbindings te vorm, insluitendyttriumoksied(Y2O3). Yttriumoksied word dikwels gebruik om fosfore en keramiek te maak.
6. ** Reaksie met sure **: yttrium kan met sterk sure reageer om ooreenstemmende soute te produseer, soosyttriumchloried (Ycl3) ofyttrium sulfaat (Y2 (SO4) 3).
7. Reaksie met water: Yttrium reageer nie direk met water onder normale omstandighede nie, maar by hoë temperature kan dit reageer met waterdamp om waterstof- en yttriumoksied te produseer.
8. Reaksie met sulfiede en karbiede: Yttrium kan met sulfiede en karbiede reageer om ooreenstemmende verbindings soos yttriumsulfied (YS) en yttriumkarbied (YC2) te vorm. 9. Isotope: Yttrium het veelvuldige isotope, waarvan die mees stabiel Yttrium-89 (^89y) is, wat 'n lang halfleeftyd het en in kerngeneeskunde en isotoop-etikettering gebruik word.
Yttrium is 'n relatiewe stabiele metaalelement met veelvuldige valensietoestande en die vermoë om met ander elemente te reageer om verbindings te vorm. Dit het 'n wye verskeidenheid toepassings in optika, materiaalwetenskap, medisyne en nywerheid, veral in fosfore, keramiekvervaardiging en lasertegnologie.
Biologiese eienskappe van yttrium
Die biologiese eienskappe vanyttriumin lewende organismes is relatief beperk.
1. Teenwoordigheid en inname: Alhoewel yttrium nie 'n element vir die lewe is nie, kan spoorhoeveelhede yttrium in die natuur voorkom, insluitend grond, rotse en water. Organismes kan spoor hoeveelhede yttrium deur die voedselketting inneem, gewoonlik van grond en plante.
2. Bio -bewerkbaarheid: Die biobeskikbaarheid van yttrium is relatief laag, wat beteken dat organismes oor die algemeen probleme ondervind om Yttrium effektief op te neem en te gebruik. Die meeste yttriumverbindings word nie maklik in organismes opgeneem nie, dus is dit geneig om uitgeskei word.
3. Verspreiding in organismes: Een keer in 'n organisme word yttrium hoofsaaklik versprei in weefsels soos die lewer, nier, milt, longe en bene. Bene bevat veral hoër konsentrasies yttrium.
4. Metabolisme en uitskeiding: Die metabolisme van yttrium in die menslike liggaam is relatief beperk omdat dit die organisme gewoonlik deur uitskeiding verlaat. Die meeste daarvan word deur urine uitgeskei, en dit kan ook in die vorm van ontlasting uitgeskei word.
5. Toksisiteit: Vanweë die lae biobeskikbaarheid daarvan, versamel Yttrium gewoonlik nie tot skadelike vlakke in normale organismes nie. Hoë dosis Yttrium-blootstelling kan egter skadelike gevolge hê vir organismes, wat tot giftige effekte kan lei. Hierdie situasie kom gewoonlik selde voor omdat yttriumkonsentrasies in die natuur gewoonlik laag is en dit nie wyd gebruik word of aan organismes blootgestel word nie. Die biologiese eienskappe van yttrium in organismes word hoofsaaklik gemanifesteer in die teenwoordigheid daarvan in spoorhoeveelhede, lae biobeskikbaarheid en is dit nie 'n element wat nodig is vir die lewe nie. Alhoewel dit onder normale omstandighede nie duidelike giftige effekte op organismes het nie, kan blootstelling aan yttrium met hoë dosisse gesondheidsgevare veroorsaak. Daarom is wetenskaplike navorsing en monitering steeds belangrik vir die veiligheid en biologiese effekte van yttrium.
Verspreiding van yttrium van aard
Yttrium is 'n seldsame aarde -element wat relatief wyd in die natuur versprei is, hoewel dit nie in suiwer elementêre vorm bestaan nie.
1. Voorkoms in die aardkors: Die oorvloed van yttrium in die aardkors is relatief laag, met 'n gemiddelde konsentrasie van ongeveer 33 mg/kg. Dit maak Yttrium een van die seldsame elemente.
Yttrium bestaan hoofsaaklik in die vorm van minerale, gewoonlik saam met ander seldsame aardelemente. Sommige belangrike yttrium -minerale sluit in Yttrium Iron Garnet (YIG) en Yttrium -oksalaat (Y2 (C2O4) 3).
2. Geografiese verspreiding: Yttrium -afsettings word oor die hele wêreld versprei, maar sommige gebiede kan ryk aan yttrium wees. Sommige belangrike Yttrium -afsettings kan in die volgende streke gevind word: Australië, China, die Verenigde State, Rusland, Kanada, Indië, Skandinawië, ens. 3. Onttrekking en verwerking: Sodra die yttrium -erts ontgin is, is chemiese verwerking gewoonlik nodig om die yttrium te onttrek en te skei. Dit behels gewoonlik suurloging en chemiese skeidingsprosesse om yttrium met 'n hoë suiwerheid te verkry.
Dit is belangrik om daarop te let dat seldsame aardelemente soos yttrium gewoonlik nie in die vorm van suiwer elemente bestaan nie, maar met ander seldsame aardelemente gemeng word. Daarom benodig die ekstraksie van yttrium met 'n hoër suiwerheid ingewikkelde chemiese verwerkings- en skeidingsprosesse. Daarbenewens is die aanbod vanSkaars aarde -elementeis beperk, dus is dit ook belangrik om hul hulpbronbestuur en omgewingsvolhoubaarheid te oorweeg.
Mynbou, ekstraksie en smelt van yttrium -element
Yttrium is 'n seldsame aarde -element wat gewoonlik nie in die vorm van suiwer yttrium bestaan nie, maar in die vorm van yttriumerts. Die volgende is 'n gedetailleerde inleiding tot die mynbou- en verfyningsproses van Yttrium -element:
1. Mynbou van yttriumerts:
Verkenning: Eerstens doen geoloë en mynbou -ingenieurs eksplorasiewerk om afsettings te vind wat yttrium bevat. Dit behels gewoonlik geologiese studies, geofisiese verkenning en steekproefanalise. Mynbou: Sodra 'n deposito wat yttrium bevat, gevind word, word die erts ontgin. Hierdie afsettings bevat gewoonlik oksiederts soos yttrium yster granaat (YIG) of yttrium -oksalaat (Y2 (C2O4) 3). Erts verplettering: Na ontginning moet die erts gewoonlik in kleiner stukke gebreek word vir daaropvolgende verwerking.
2. Uittreksel van yttrium:Chemiese loging: Die fyngemaakte erts word gewoonlik na 'n smelter gestuur, waar yttrium deur chemiese loging onttrek word. Hierdie proses gebruik gewoonlik 'n suur loogoplossing, soos swaelsuur, om die yttrium van die erts op te los. Skeiding: Sodra Yttrium opgelos is, word dit gewoonlik gemeng met ander seldsame aardelemente en onsuiwerhede. Ten einde yttrium van hoër suiwerheid te onttrek, is 'n skeidingsproses nodig, gewoonlik met behulp van oplosmiddel -ekstraksie, ioonuitruiling of ander chemiese metodes. Neerslag: Yttrium word geskei van ander seldsame aardelemente deur toepaslike chemiese reaksies om suiwer yttriumverbindings te vorm. Droging en kalsinering: Die verkrygde yttriumverbindings moet gewoonlik gedroog en gekalsineer word om enige oorblywende vog en onsuiwerhede te verwyder om uiteindelik suiwer yttriummetaal of verbindings te verkry.
Opsporingsmetodes van yttrium
Algemene opsporingsmetodes vir yttrium sluit hoofsaaklik atoomabsorpsiespektroskopie (AAS), induktief gekoppelde plasma-massaspektrometrie (ICP-MS), X-straal-fluorescentiespektroskopie (XRF), ens.
1. Atoomabsorpsiespektroskopie (AAS):AAS is 'n algemeen gebruikte kwantitatiewe analise -metode wat geskik is vir die bepaling van die Yttrium -inhoud in oplossing. Hierdie metode is gebaseer op die absorpsieverskynsel wanneer die teikenelement in die monster lig van 'n spesifieke golflengte absorbeer. Eerstens word die monster omgeskakel in 'n meetbare vorm deur voorbehandelingstappe soos gasverbranding en droging met 'n hoë temperatuur. Daarna word lig wat ooreenstem met die golflengte van die teikenelement in die monster, die ligintensiteit wat deur die monster opgeneem word, gemeet, en die yttriuminhoud in die monster word bereken deur dit met 'n standaard yttrium -oplossing van bekende konsentrasie te vergelyk.
2. induktief gekoppelde plasma-massaspektrometrie (ICP-MS):ICP-MS is 'n baie sensitiewe analitiese tegniek wat geskik is vir die bepaling van die yttriuminhoud in vloeistof- en vaste monsters. Hierdie metode omskakel die monster in gelaaide deeltjies en gebruik dan 'n massaspektrometer vir massa -analise. ICP-MS het 'n wye opsporingsreeks en 'n hoë resolusie, en kan die inhoud van veelvuldige elemente tegelyk bepaal. Vir die opsporing van Yttrium kan ICP-MS baie lae opsporingsgrense en hoë akkuraatheid bied.
3. X-straal fluorescentiespektrometrie (XRF):XRF is 'n nie-vernietigende analitiese metode wat geskik is vir die bepaling van yttriuminhoud in vaste en vloeibare monsters. Hierdie metode bepaal die elementinhoud deur die oppervlak van die monster met x-strale te bestraal en die kenmerkende piekintensiteit van die fluorescentie-spektrum in die monster te meet. XRF het die voordele van vinnige snelheid, eenvoudige werking en die vermoë om verskeie elemente terselfdertyd te bepaal. Daar kan egter met XRF inmeng word in die ontleding van yttrium met 'n lae inhoud, wat groot foute tot gevolg het.
4. induktief gekoppelde plasma-optiese emissiespektrometrie (ICP-OES):Induktief gekoppelde plasma-optiese emissiespektrometrie is 'n baie sensitiewe en selektiewe analitiese metode wat wyd gebruik word in multi-element-analise. Dit atomiseer die monster en vorm 'n plasma om die spesifieke golflengte en intensiteit O te meetf yttriumemissie in die spektrometer. Benewens bogenoemde metodes, is daar ander algemeen gebruikte metodes vir yttrium -opsporing, insluitend elektrochemiese metode, spektrofotometrie, ens. Die seleksie van 'n geskikte opsporingsmetode hang af van faktore soos monstereienskappe, die vereiste meetbereik en opsporing van die akkuraatheid en die kaliberingsstandaarde is dikwels nodig vir kwaliteitskontrole om die akkuraatheid en betroubaarheid van die meetresultate te verseker.
Spesifieke toepassing van yttrium atoomabsorpsiemetode
In elementmeting is induktief gekoppelde plasma-massaspektrometrie (ICP-MS) 'n baie sensitiewe en multi-element-analise-tegniek, wat dikwels gebruik word om die konsentrasie van elemente, insluitend yttrium, te bepaal. Die volgende is 'n gedetailleerde proses vir die toets van yttrium in ICP-MS:
1. Voorbereiding van monster:
Die monster moet gewoonlik opgelos word of in 'n vloeibare vorm versprei word vir ICP-MS-analise. Dit kan gedoen word deur chemiese ontbinding, vertering van die verhitting of ander toepaslike voorbereidingsmetodes.
Die voorbereiding van die monster benodig uiters skoon toestande om besoedeling deur enige eksterne elemente te voorkom. Die laboratorium moet die nodige maatreëls tref om monsterbesoedeling te voorkom.
2. ICP Generation:
ICP word gegenereer deur argon- of argon-suurstof gemengde gas in 'n geslote kwartsplasma-fakkel in te voer. Hoëfrekwensie-induktiewe koppeling lewer 'n intense plasma-vlam, wat die beginpunt van die ontleding is.
Die temperatuur van die plasma is ongeveer 8000 tot 10000 grade Celsius, wat hoog genoeg is om die elemente in die monster in ioniese toestand te omskep.
3. Ionisasie en skeiding:Sodra die monster die plasma binnedring, is die elemente daarin geïoniseerd. Dit beteken dat die atome een of meer elektrone verloor en gelaaide ione vorm. ICP-MS gebruik 'n massaspektrometer om die ione van verskillende elemente te skei, gewoonlik volgens massa-tot-lading-verhouding (M/Z). Hiermee kan die ione van verskillende elemente geskei word en daarna ontleed word.
4. massaspektrometrie:Die geskeide ione voer 'n massaspektrometer in, gewoonlik 'n viervoudige massaspektrometer of 'n magnetiese skanderingsmassaspektrometer. In die massaspektrometer word die ione van verskillende elemente van mekaar geskei en opgespoor volgens hul massa-tot-lading-verhouding. Dit laat die teenwoordigheid en konsentrasie van elke element bepaal. Een van die voordele van induktief gekoppelde plasma -massaspektrometrie is die hoë resolusie, wat dit in staat stel om verskeie elemente gelyktydig op te spoor.
5. Dataverwerking:Die data wat deur ICP-MS gegenereer word, moet gewoonlik verwerk en geanaliseer word om die konsentrasie van die elemente in die monster te bepaal. Dit sluit in die vergelyking van die opsporingsein volgens standaarde van bekende konsentrasies, en die uitvoering van kalibrasie en regstelling.
6. Resultaatverslag:Die finale resultaat word aangebied as die konsentrasie of massa -persentasie van die element. Hierdie resultate kan gebruik word in 'n verskeidenheid toepassings, insluitend aardwetenskap, omgewingsanalise, voedseltoetsing, mediese navorsing, ens.
ICP-MS is 'n hoogs akkurate en sensitiewe tegniek wat geskik is vir multi-element-analise, insluitend yttrium. Dit verg egter ingewikkelde instrumente en kundigheid, dus word dit gewoonlik in 'n laboratorium of 'n professionele ontledingsentrum uitgevoer. In werklike werk is dit nodig om die toepaslike meetmetode volgens die spesifieke behoeftes van die webwerf te kies. Hierdie metodes word wyd gebruik in die ontleding en opsporing van Ytterbium in laboratoriums en nywerhede.
Nadat ons bogenoemde opgesom het, kan ons aflei dat Yttrium 'n baie interessante chemiese element is met unieke fisiese en chemiese eienskappe, wat van groot belang is in wetenskaplike navorsing en toepassingsvelde. Alhoewel ons 'n mate van vordering gemaak het in ons begrip daarvan, is daar nog baie vrae wat verdere navorsing en verkenning benodig. Ek hoop dat ons inleiding lesers kan help om hierdie fassinerende element beter te verstaan en almal se liefde vir wetenskap en belangstelling in verkenning te inspireer.
Vir meer inligting plsKontak onsOnder:
Tel & whats: 008613524231522
Email:Sales@shxlchem.com
Postyd: Nov-28-2024