ඔයා දැනගෙන හිටියා ද? සොයා ගන්නා මිනිසුන්ගේ ක්රියාවලියyttriumවිකෘති හා අභියෝග වලින් පිරී තිබුණි. 1787 දී ස්වීඩේ කාල් ඇක්සෙල් අර්හියස් සිය උපන් ගම වන යට්terby ගම්මානය අසල ගල් වළක effect න හා බර කළු ලෝහයක් අහම්බෙන් සොයා ගත් අතර එය "YTTTERBITE" ලෙස නම් කළේය. ඊට පසු, ජොහාන් ගඩොලිලින්, ඇන්ඩර්ස් ගුස්ටව් එක්බර්ග්, ෆ්රෙඩ්රික් වල්ර් සහ අනෙක් අය ඇතුළු බොහෝ විද්යා scientists යන් ඇතුළු බොහෝ විද්යා scientists යන් මෙම යහරි පිළිබඳ ගැඹුරින් පර්යේෂණ සිදු කළහ.
1794 දී ෆින්ලන්ත රසායන mist ජොහාන් ගඩොලින් යට්ටර්බියම් ඔක්කුවේ නව ඔක්සයිඩ් නව ඔක්සයිඩ් සාර්ථකව වෙන් කර එය yttrium ලෙස නම් කළේය. දුර්ලභ පස් මූලද්රව්යයක් මිනිසුන් පැහැදිලිවම සොයා ගත් පළමු අවස්ථාව මෙයයි. කෙසේ වෙතත්, මෙම සොයා ගැනීම වහාම පුළුල් අවධානය යොමු නොවීය.
කාලයාගේ ඇවෑමෙන් විද්යා scientists යින් වෙනත් දුර්ලභ පෘථිවි මූලද්රව්ය සොයාගෙන ඇත. 1803 දී ජර්මානු ක්ලැප්රෝත් සහ ස්වීඩන් හිට්සින්ගර් සහ බෙස්ලියස් සීරියම් සොයා ගත්හ. 1839 දී ස්වීඩේ මොසැන්ඩර් සොයා ගන්නා ලදීලැන්තනම්. 1843 දී ඔහු erbyium සොයා ගත්තේයටර්බියම්. මෙම සොයාගැනීම් නිසා පසුව විද්යාත්මක පර්යේෂණ සඳහා වැදගත් පදනමක් ලබා දුන්නේය.
19 වන ශතවර්ෂයේ අවසානය දක්වාම විද්යා scientists යින් යෙට්රීම් ලෝපස් වෙතින් "යෙට්රියම්" මූලද්රව්යය සාර්ථකව වෙන් කිරීමත් නොවේ. 1885 දී ඔස්ට්රියානු විල්ස්බැක් විසින් නීෝඩිමියම් සහ ප්රවීරියම් සොයා ගන්නා ලදී. 1886 දී බොයිස් බෞද්ධයා සොයා ගන්නා ලදීඩිස්ප්රොෆියම්. මෙම සොයාගැනීම් නිසා දුර්ලභ පෘථිවි මූලද්රව්ය විශාල පවුලක් තවදුරටත් පොහොසත් කළේය.
YTTrium සොයාගැනීමෙන් පසු ශතවර්ෂයකට වැඩි කාලයක්, තාක්ෂණික තත්වයේ සීමාවන් නිසා, විද්යා scientists යින්ට මෙම අංගය පිරිසිදු කිරීමට නොහැකි වී ඇති අතර, එය සමහර ශාස්ත්රීය ආරවුල් සහ දෝෂ ද ඇති කර තිබේ. කෙසේ වෙතත්, විද්යා scientists යින් යෙට්රීම් අධ්යයනය කිරීම සඳහා ඔවුන්ගේ උද්යෝගයෙන් නතර නොවීය.
විසිවන සියවසේ මුල් භාගයේදී විද්යා හා තාක්ෂණ අඛණ්ඩව දියුණු දියුණුවත් සමඟ විද්යා scientists යින් අවසානයේ දුර්ලභ පෘථිවි මූලද්රව්ය පිරිසිදු කිරීමට හැකි වනු ඇත. 1901 දී ප්රංශ ජාතික ඉයුජින් ඩි මර්සෙයිල් විසින් සොයා ගන්නා ලදීයුරෝපියාව. 1907-1908 දී ඔස්ට්රියානු විල්ස්බැක් සහ ප්රංශ ජාතික ස්වාකයකු ස්වාධීනව ලුතෙටියම් සොයා ගන්නා ලදී. මෙම සොයාගැනීම් නිසා පසුව විද්යාත්මක පර්යේෂණ සඳහා වැදගත් පදනමක් ලබා දුන්නේය.
නූතන විද්යාවේ හා තාක්ෂණයෙන්, yttrium යෙදීමෙන් වැඩි වැඩියෙන් පුළුල් වෙමින් පවතී. විද්යාවේ හා තාක්ෂණයේ අඛණ්ඩ දියුණුවත් සමඟ, අපගේ අවබෝධය සහ යෙට්රම්ගේ අවබෝධය හා යෙදුම වැඩි වැඩියෙන් ගැඹුරින් වැටෙනු ඇත.
යෙට්රම් මූලද්රව්යයේ යෙදුම් ක්ෂේත්ර
1.දෘශ්ය වීදුරු සහ පිඟන් මැටි:දෘශ්ය වීදුරු හා පිඟන් මැටි නිෂ්පාදනය සඳහා YTTRUM බහුලව භාවිතා වේ. ප්රධාන වශයෙන් විනිවිද පෙනෙන පිණිස සහ දෘශ්ය වීදුරු නිෂ්පාදනය සඳහා. එහි සංයෝගවල විශිෂ්ට දෘශ්ය ගුණාංග ඇති අතර ලේසර්, ෆයිබර්-ඔප්ටික් සන්නිවේදන සහ වෙනත් උපකරණවල සංරචක නිෂ්පාදනය කිරීම සඳහා භාවිතා කළ හැකිය.
2. පොස්පීර්ස්:YTTrium සංයෝග පොස්පරස් හි වැදගත් කාර්යභාරයක් ඉටු කරන අතර දීප්තිමත් ප්රතිදීප්ත විමෝචනය කළ හැකි බැවින් ඒවා බොහෝ විට රූපවාහිනී තිර, මොනිටර සහ ආලෝකකරණ උපකරණ නිෂ්පාදනය කිරීම සඳහා බොහෝ විට භාවිතා වේ.Yttrium oxideඅනෙකුත් සංයෝග බොහෝ විට ආලෝකයේ දීප්තිය සහ පැහැදිලිකම වැඩි දියුණු කිරීම සඳහා දීප්සීනට් ද්රව්ය ලෙස භාවිතා කරයි.
3. මිශ්ර ලෝහ ආහික්: ලෝහ මිශ්ර ලෝහ නිෂ්පාදනය කිරීමේදී, YTTRIM බොහෝ විට ආකලන ගුණාංග හා ලෝහවල විඛාදන ප්රතිරෝධය වැඩි දියුණු කිරීම සඳහා ආකලන ලෙස භාවිතා කරයි.Yttrium alloysබොහෝ විට ඉහළ ශක්තියක් සහිත වානේ සෑදීමට භාවිතා කරයිඇලුමිනියම් මිශ්ර ලෝහ, ඒවා වඩාත් තාප ප්රතිරෝධී හා විඛාදන හා ප්රතිරෝධී වේ.
4. උත්ප්රේරක: YTTrium සංයෝග සමහර උත්ප්රේරක වල වැදගත් කාර්යභාරයක් ඉටු කරන අතර රසායනික ප්රතික්රියා අනුපාතය වේගවත් කළ හැකිය. කාර්මික නිෂ්පාදන ක්රියාවලීන්හි මෝටර් රථ පිටාර පිරිසිදු කිරීමේ උපකරණ සහ උත්ප්රේරක නිෂ්පාදනය සඳහා ඒවා භාවිතා කරන අතර හානිකර ද්රව්ය විමෝචනය කිරීම අඩු කිරීමට උපකාරී වේ.
5. වෛද්ය නිරූපණ තාක්ෂණය: වෛද්ය නිරූපණ තාක්ෂණයේ විකිරණශීලී සමස්ථානිකවල විකිරණශීලී සමස්ථානිකවල විකිරණශීලී සමස්ථානික සකස් කිරීම සහ න්යෂ්ටික වෛද්ය රූපකරණය හඳුනා ගැනීම වැනි විකිරණශීලී සමස්ථානික සකස් කිරීම සඳහා YTTrium සමස්ථානික භාවිතා වේ.
6. ලේසර් තාක්ෂණය:YTTrium අයන ලේසර් යනු විවිධ විද්යාත්මක පර්යේෂණ, ලේසර් medicine ෂධ සහ කාර්මික යෙදුම් සඳහා භාවිතා කරන පොදු රාජ්ය ලේසර් ය. මෙම ලේසර් නිෂ්පාදනය කිරීම සඳහා සක්රියර් ලෙස ඇතැම් YTTrium සංයෝග භාවිතා කිරීම අවශ්ය වේ.යිට්රියම් මූලද්රව්යදෘෂ්ටි, ද්රව්ය විද්යාව සහ medicine ෂධ වැනි බොහෝ ක්ෂේත්ර සම්බන්ධ වන අතර මානව සමාජයේ ප්රගතිය හා සංවර්ධනය සඳහා ඔවුන්ගේ ප්රධාන විද්යාවේ හා තාක්ෂණය හා කර්මාන්තයේ ඔවුන්ගේ සංයෝග වැදගත් කාර්යභාරයක් ඉටු කරයි.
YTTrium හි භෞතික ගුණාංග
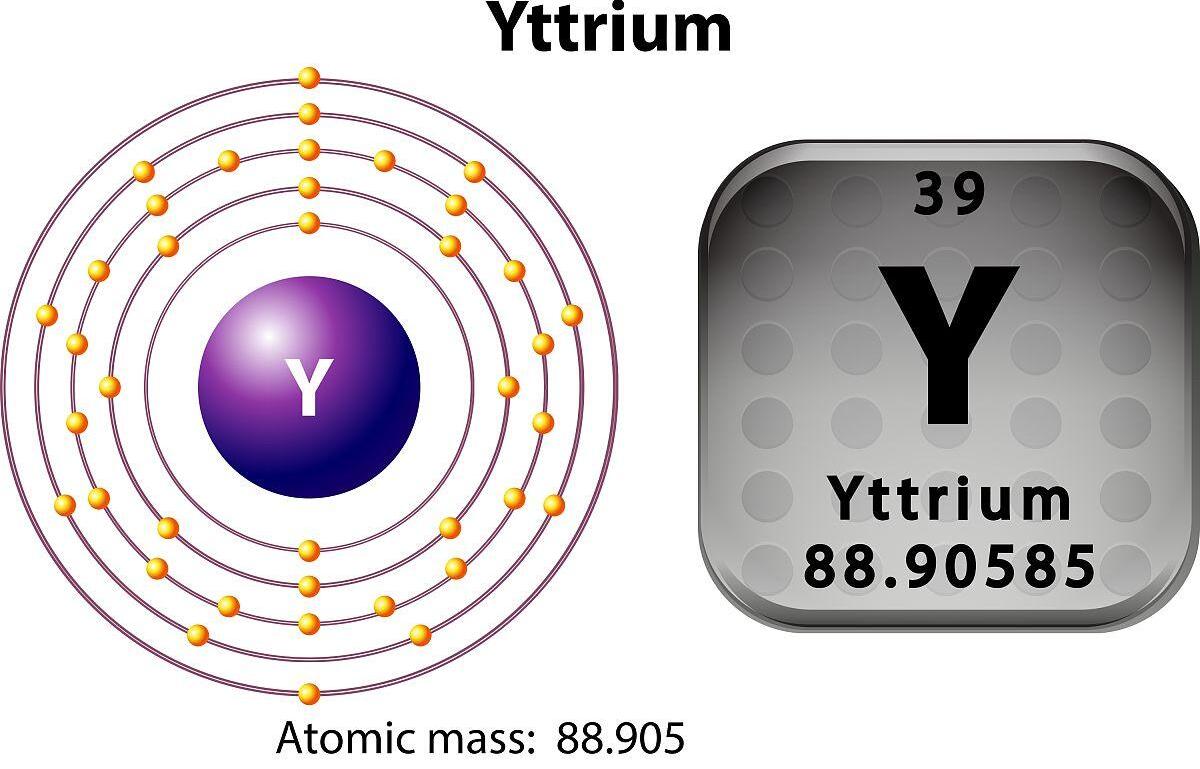
පරමාණුක ගණනyttrium39 සහ එහි රසායනික සංකේතය y වේ.
1. පෙනුම:Yttrium යනු රිදී-සුදු ලෝහයකි.
2. ity නත්වය:YTTrium හි ity නත්වය 4.47 g / cm3 වන අතර එමඟින් පෘථිවි පෘෂ් .යේ සාපේක්ෂව බර මූලද්රව්ය වලින් එකකි.
3. දියවන ස්ථානය:යෙට්රීම් හි ද්රවාංකයේ දියවීම සෙල්සියස් අංශක 1522 (FAHRENHEIIT අංශක 2782) වන අතර, එමඟින් යුධ සමයේ තාප තත්වයන් යටතේ YTTRIM සිට ද්රව තත්වයට වෙනස් වේ.
4. තාපාංකය:යට්රියම් හි තාපාංකය සෙල්සියස් අංශක 3336 ක් (ෆැරන්හයිට් අංශක 6037) වන අතර, එමඟින් තාප තත්වයන් යටතේ යත්රයකින් ද්රව තත්වයක් ඇති වන උෂ්ණත්වය ගැන සඳහන් වේ.
5. අදියර:කාමර උෂ්ණත්වයේ දී, YTTRIM state න තත්වයක පවතී.
6. සන්නායකතාව:YTTRUM යනු ඉහළ සන්නායකතාවයකින් යුත් විදුලි සන්නායකයක් වන බැවින් ඉලෙක්ට්රොනික උපාංග නිෂ්පාදන හා පරිපථ තාක්ෂණයේ ඇතැම් යෙදුම් ඇත.
7. චුම්භකත්වය:YTTRUM යනු කාමර උෂ්ණත්වයේ දී පරාමිතික ද්රව්යයකි, එයින් අදහස් කරන්නේ එය චුම්බක ක්ෂේත්රවලට පැහැදිලි චුම්බක ප්රතිචාරයක් නොමැති බවයි.
8. ස් stal ටික ව්යුහය: Yttrum හෙක්සකර්ග්නල් කිට්ටු ඇසුරුම් කළ ස් stal ටික ව්යුහයක් තුළ පවතී.
9. පරමාණුක පරිමාව:යෙට්රම් හි පරමාණුක පරිමාව මවුලයකට cub න සෙන්ටිමීටර 19.8 කි.
YTTRIM යනු සාපේක්ෂව ඉහළ dens නත්වය හා ද්රවාංකයක් ඇති අතර හොඳ සන්නායකතාවක් ඇති ලෝහමය අංගයකි, එබැවින් එයට ඉලෙක්ට්රොනික උපකරණ, ද්රව්ය විද්යාව සහ වෙනත් ක්ෂේත්රවල වැදගත් යෙදුම් ඇත. ඒ අතරම, YTTrum ද සාපේක්ෂව පොදු දුර්ලභ අංගයකි, එය සමහර උසස් තාක්ෂණයන් හා කාර්මික යෙදුම් වල වැදගත් කාර්යභාරයක් ඉටු කරයි.
YTTrium හි රසායනික ගුණාංග
1. රසායනික සංකේතය සහ සමූහය: YTTrium හි රසායනික සංකේතය y යනු වන අතර එය ආවරණ වගුවේ පස්වන කාල පරිච්ඡේදයේ, තෙවැනි කණ්ඩායමේ පස්වන කාල පරිච්ඡේදයේ, එය ලැන්තනීසයිඩ් මූලද්රව්යයන්ට සමාන වේ.
2. ඉලෙක්ට්රොනික් ව්යුහය: yttrium හි විද්යුත් ව්යුහය 1s² 2s² 2p⁶ 3p⁶ 3p⁶ 3p⁶ 4p⁶ 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5S² 5s² 5s² පිටත ඉලෙක්ට්රෝන ස්ථරයේ, යෙට්රම් වලට සංයුජතා ඉලෙක්ට්රෝන දෙකක් ඇත.
3. වැලෙන්ස් ප්රාන්තය: YTTRIM සාමාන්යයෙන් පෙන්නුම් කරන්නේ සාමාන්යයෙන් +3 හි සංයුජතා තත්වයක් වන අතර එය වඩාත් සුලභ සංයුජතා තත්වය වන නමුත් +2 සහ +1 හි සංයුජතා තත්වයන් ද පෙන්විය හැකිය.
4. ප්රතික්රියාකාරිත්වය: yttrum සාපේක්ෂව ස්ථාවර ලෝහයක් වන නමුත් එය වාතයට නිරාවරණය වන විට ක්රමයෙන් ඔක්සිකරණය වේ, මතුපිට ඔක්සයිඩ් තට්ටුවක් සෑදීම. මෙට්ට්රියම් එහි දීප්තිය නැති වී යයි. YTTrium ආරක්ෂා කිරීම සඳහා, එය සාමාන්යයෙන් වියළි පරිසරයක ගබඩා වේ.
5. ඔක්සයිඩ් සමඟ ප්රතික්රියා කිරීම: විවිධ සංයෝග ඇතුළුව විවිධ සංයෝග සෑදීමට YTTrium ප්රතික්රියා කරයිyttrium oxide(Y2o3). YTTRium oxide බොහෝ විට පොස්පරස් සහ පිඟන් මැටි සෑදීම සඳහා භාවිතා කරයි.
6. ** අම්ල සමඟ ප්රතික්රියාව **: YTTRUM ට ශක්තිමත් අම්ල සමඟ ප්රතික්රියා කළ හැකිය, වැනි අනුරූප ලවණ නිෂ්පාදනය කිරීමටYTTRIM ක්ලෝරයිඩ් (Ycl3) හෝyttrium sulfate (Y2 (SO4) 3).
7. ජලය සමග ප්රතික්රියා කිරීම: සාමාන්ය තත්වයන් යටතේ YTTRUM සෘජුවම ජලය සමඟ කෙලින්ම ප්රතික්රියා නොකරන නමුත් ඉහළ උෂ්ණත්වවලදී, හයිඩ්රජන් සහ YTTrium ඔක්සයිඩ් නිපදවීම සඳහා ජල වාෂ්ප සමඟ එය ප්රතික්රියා කළ හැකිය.
8. සල්ෆයිඩ් සහ කාබයිඩ් සමඟ ප්රතික්රියා කිරීම: YTTRYUM සල්ෆයිඩ් (YS) සහ YTTRium CABIDE (YC2) වැනි අනුරූපී සංයෝග සෑදීම සඳහා YTTRIM සහ CARBIDS සමඟ ප්රතික්රියා කළ හැකිය. 9. සමස්ථානික: YTTROUM ඇත: YTTrum සතුව බහු අවයවයක් ඇති අතර, දිගු අර්ධ ආයු කාලයක් ඇති yttrium-89 (^ 89y) වන අතර න්යෂ්ටික medicine ෂධයේ සහ සමස්ථානික ලේබල් කිරීම සඳහා භාවිතා වේ.
Yttrium යනු බහු සංයුතිමත් තත්වයක් ඇති සාපේක්ෂව ස්ථායී ලෝහමය අංගයක් වන අතර සංයෝග සෑදීම සඳහා වෙනත් මූලද්රව්ය සමඟ ප්රතික්රියා කිරීමේ හැකියාව. දෘෂ්ටි, ද්රව්ය විද්යාව, වෛද්ය විද්යාව සහ කර්මාන්තයේ, විශේෂයෙන් ෆොස්ෆෝර්ස්, පිඟන් මැටි නිෂ්පාදන සහ ලේසර් තාක්ෂණය යන දෘෂ්ටි, ද්රව්ය, medicine ෂධ සහ කර්මාන්තවල පුළුල් පරාසයක යෙදුම් එහි ඇත.
YTTrium හි ජීව විද්යාත්මක ගුණාංග
හි ජීව විද්යාත්මක ගුණyttriumජීවීන් තුළ සාපේක්ෂව සීමිතය.
1. පැමිණීම සහ ශරීරගත කිරීම: yttrum ජීවිතයට අත්යවශ්ය අංගයක් නොවූවත්, YTTrium පස, පාෂාණ සහ ජලය ඇතුළු YTTrim ප්රමාණය සොයා ගත හැකිය. ජීවීන්ට සාමාන්යයෙන් පාංශු හා ශාක වලින් ආහාර දාමය හරහා YTTrium වල YTTRAM ප්රමාණයක් ලබා ගත හැකිය.
2. ජෛව නියාවෙන්: YTTrium හි චෛර්ය විද්යාව සාපේක්ෂව අඩු ය, එයින් අදහස් කරන්නේ ජීවීන්ට සාමාන්යයෙන් සාමාන්යයෙන් YTTrium effectively ලදායී ලෙස අවශෝෂණය කර භාවිතා කිරීමට අපහසු බවයි. බොහෝ yttrium සංයෝග පහසුවෙන් ජීවත්වන බැවින් ඒවා බැහැර කිරීමට නැඹුරු වේ.
3. ජීවීන්ගේ බෙදා හැරීම: ජීරියාවක එක් වරක්, YTTRium ප්රධාන වශයෙන් බෙදා හරිනු ලැබේ, වකුගඩු, වකුගඩු, ප්ලීහාව, පෙනහළු, පෙණහලු සහ ඇටකටු වැනි පටක වලින්. විශේෂයෙන්, අස්ථිවල YTTRAM හි ඉහළ සාන්ද්රණයක් අඩංගු වේ.
4. පරිවෘත්තීය හා බැහැර කිරීම: මිනිස් සිරුරේ YTTrium හි පරිවෘත්තීය සාපේක්ෂව සීමිත වන්නේ එය සාමාන්යයෙන් ජීවියාට බැහැර කිරීම නිසාය. එයින් වැඩි ප්රමාණයක් මුත්රා හරහා බැහැර කරන අතර, එය මිරිකීම පිළිබඳ ස්වරූපයෙන් බැහැර කළ හැකිය.
5. විෂ වීම: එහි අඩු ජෛවපදාව නිසා, YTTRIM සාමාන්යයෙන් සාමාන්ය ජීවීන්ගේ හානිකර මට්ටමට එකතු නොවේ. කෙසේ වෙතත්, ඉහළ මාත්රාව යෙට්රම් නිරාවරණය මගින් ජීවීන්ට හානිකර බලපෑම් වලට හානිකර බලපෑම් ඇති විය හැකිය. මෙම තත්වය සාමාන්යයෙන් සිදු වන්නේ කලාතුරකිනි, සොබාදහමේ YTTrium සාන්ද්රණය සාමාන්යයෙන් අඩු වන අතර එය ජීවීන්ට බහුලව භාවිතා නොකෙරේ හෝ ජීවීන්ට නිරාවරණය නොවේ. සාමාන්ය තත්වයන් යටතේ ජීවීන්ට පැහැදිලිව පෙනෙන විෂ සහිත බලපෑමක් නොතිබුණද, ඉහළ මාත්රාව යෙට්රම් නිරාවරණය සෞඛ්ය උපද්රව ඇති විය හැක. එබැවින් විද්යාත්මක පර්යේෂණ හා අධීක්ෂණය යට්රියම් වල ආරක්ෂාව සහ ජීව විද්යාත්මක බලපෑම් සඳහා තවමත් වැදගත් ය.
සොබාදහමේ YTTrium බෙදා හැරීම
Yttrum යනු සොබාදහමේ සාපේක්ෂව සොබාදහමේ සාපේක්ෂව බහුලව බෙදා හරින ලද දුර්ලභ පෘථිවි මූලද්රව්යයකි, එය පිරිසිදු මූලද්රව්ය ස්වරූපයෙන් නොපවතී.
1. පෘථිවි කබොලෙහි සිදුවීම: පෘථිවි පෘෂ් .යේ YTTrium හි බහුලත්වය සාපේක්ෂව අඩු වන අතර සාමාන්ය සාන්ද්රණය 33 mg / kg පමණ වේ. මෙය දුර්ලභ අංග වලින් එකක් බවට පත් කරයි.
YTTRIM ප්රධාන වශයෙන් ඛනිජ ස්වරූපයෙන් පවතී, සාමාන්යයෙන් වෙනත් දුර්ලභ පෘථිවි මූලද්රව්ය සමඟ. සමහර ප්රධාන yttrium ඛනිජ ඇතුළත් වේ yttrium යකඩ ගාර්නෙට් (යෙට්රීම් යකඩ ගාර්නට් (YIG) සහ yttrium oxlaate (Y2 (C2O4) 3).
2. භූගෝලීය ව්යාප්තිය: yttrium තැන්පතු ලොව පුරා බෙදා හරිනු ලැබේ, නමුත් සමහර ප්රදේශ යිට්රියම් වලින් පොහොසත් විය හැකිය. සමහර ප්රධාන yttrium තැන්පතු පහත සඳහන් කලාපවල සොයාගත හැකිය: ඕස්ට්රේලියාව, චීනය, කැනඩාව, ඉන්දියාව, ඉන්දියාව, ස්කැන්ඩිනේවිය, ස්කැන්ඩිනේවිය, ඊ.ආර්.ඊ. මෙම සාමාන්යයෙන් උස් සංශුද්ධතා යට්රියම් ලබා ගැනීම සඳහා අම්ල කාන්දු වන හා රසායනික වෙන් කිරීමේ ක්රියාවලීන් ඇතුළත් වේ.
YTTrium වැනි දුර්ලභ පෘථිවි මූලද්රව්යයන් සාමාන්යයෙන් පිරිසිදු මූලද්රව්ය ස්වරූපයෙන් නොපවතින නමුත් වෙනත් දුර්ලභ පෘථිවි මූලද්රව්ය සමඟ මිශ්ර වී ඇති බව සැලකිල්ලට ගැනීම වැදගත්ය. එබැවින්, ඉහළ සංශුද්ධතාවය YTTRIM නිස්සාරණය කිරීම සඳහා සංකීර්ණ රසායනික සැකසුම් හා වෙන් කිරීමේ ක්රියාවලීන් අවශ්ය වේ. ඊට අමතරව, සැපයුමදුර්ලභ පෘථිවි මූලද්රව්යසීමිතයි, එබැවින් ඔවුන්ගේ සම්පත් කළමනාකරණය සහ පාරිසරික තිරසාරභාවය ගැන සලකා බැලීම ද වැදගත් ය.
YTTrium මූලද්රව්යය පතල් කැණීම, නිස්සාරණය කිරීම සහ උණු කිරීම
YTTRIM යනු සාමාන්යයෙන් පිරිසිදු යත්රම් ස්වරූපයෙන් නොපවතින දුර්ලභ පස් මූලද්රව්යයකි, නමුත් YTTrium ලෝපස් ස්වරූපයෙන්. පහත දැක්වෙන්නේ YTTrium මූලද්රව්යයේ පතල් කැණීම් සහ පිරිපහදු කිරීමේ ක්රියාවලිය පිළිබඳ සවිස්තරාත්මක හැඳින්වීමකි:
1. YTTrium ore හි පතල් කැණීම:
ගවේෂණය: පළමුව, භූ විද්යා ologists යින් සහ පතල් ඉංජිනේරුවන් යට්රියම් අඩංගු තැන්පතු සොයා ගැනීම සඳහා ගවේෂණ වැඩ කරති. මෙයට සාමාන්යයෙන් භූ විද්යාත්මක අධ්යයන, භූ භෞතික ගවේෂණය සහ නියැදි විශ්ලේෂණය ඇතුළත් වේ. පතල් කැණීම: yttrium අඩංගු තැන්පතුවක් හමු වූ පසු, ලෝපස් හෑරීම. මෙම තැන්පතු සාමාන්යයෙන් YTTrium යකඩ ගංන (යෙට්රීම් යකඩ ගංන (යූපා) හෝ YTTRYUM OXLATATE (Y2 (C2O4) 3 වැනි ඔක්සයිඩ් ලෝපස් ඇතුළත් වේ). ලෝපස් තලා දැමීම: පතල් කැණීමෙන් පසු, පසුව සැකසුම් කිරීම සඳහා ලෝපස් සාමාන්යයෙන් කුඩා කැබලිවලට කුඩා කැබලිවලට කැඩී යා යුතුය.
2. යට්රියම් නිස්සාරණය කිරීම:රසායනික කාන්දු වීම: තැළුණු ලෝපස් සාමාන්යයෙන් සුවඳකට යවනු ලැබේ, එහිදී YTTrium රසායනික කාන්දු වීම තුළින් නිස්සාරණය කරනු ලැබේ. මෙම ක්රියාවලිය සාමාන්යයෙන් යට්රියම් යට්රියම් විසුරුවා හැරීම සඳහා සල්ෆියුරික් අම්ලය වැනි ආම්ලික කාන්දු වීමේ ද්රාවණයක් භාවිතා කරයි. වෙන්වීම: YTTrum විසුරුවා හැරීමෙන් පසු එය සාමාන්යයෙන් වෙනත් දුර්ලභ පෘථිවි අංග සහ අපද්රව්ය සමඟ මිශ්ර වේ. ඉහළ සංශුද්ධතාවයේ Yttrium නිස්සාරණය කිරීම සඳහා, සාමාන්යයෙන් ද්රාවක නිස්සාරණය, අයන හුවමාරුව හෝ වෙනත් රසායනික ක්රම භාවිතා කරමින් වෙන්වීමේ ක්රියාවලියක් අවශ්ය වේ. වර්ෂාපතනය: YTTRium පිරිසිදු රසායනික ප්රතික්රියා තුළින් පිරිසිදු රසායනික ප්රතික්රියා තුළින් වෙනත් දුර්ලභ පෘථිවියෙන් වෙන් කරනු ලැබේ. වියළීම සහ කැල්වීම: ලබාගත් YTTrium සංයෝග සාමාන්යයෙන් වියළන ලද අතර පිරිසිදු යෙට්රම් ලෝහ හෝ සංයෝග ලබා ගැනීම සඳහා ඕනෑම අවශේෂ තෙතමනය හා අපද්රව්ය ඉවත් කිරීම සඳහා ගණනය කළ යුතු අතර ගණනය කළ යුතුය.
YTTrium හි හඳුනාගැනීමේ ක්රම
YTTrium සඳහා පොදු අනාවරක ක්රම ප්රධාන වශයෙන් පරමාණුක අවශෝෂණය, වර්ණාවලීක්ෂයේ වර්ණාවලීක්ෂය (AAS), ප්රේරක ජනප්රිය වර්ණාවලීක්ෂය (ICRF MS), එක්ස් කිරණ ප්රතිදීප්ත වර්ණාවලිය (එක්ස්ආර්එෆ්) ආදිය.
1. පරමාණුක අවශෝෂණ වර්ණාවලීක්ෂය (AAS):AAS යනු විසඳුමේ YTTrium අන්තර්ගතය තීරණය කිරීම සඳහා සුදුසු තරම් භාවිතා කළ ප්රමාණාත්මක විශ්ලේෂණ ක්රමයකි. නියැදියේ ඉලක්කගත මූලද්රව්යය නිශ්චිත තරංග ආයාමයක ආලෝකය අවශෝෂණය කරන විට මෙම ක්රමය අවශෝෂණ සංසිද්ධිය මත පදනම් වේ. පළමුව, වාෂ්ප, ගෑස් දහනය සහ ඉහළ උෂ්ණත්ව වියළීම වැනි පූර්ව ප්රතිකාර පියවර මගින් නියැදිය මනිනුකූල ස්වරූපයක් බවට පරිවර්තනය වේ. එවිට, ඉලක්කයේ මූලද්රව්යයේ තරංග ආයාමය සඳහා අනුරූප වන ආලෝකය සාම්පලයට සම්ප්රේෂණය වන අතර, නියැදිය මගින් ආලෝකයේ තීව්රතාවය අවශෝෂණය කර ගන්නා අතර නියැදියේ YTTrium අන්තර්ගතය දන්නා සාන්ද්රණයේ සම්මත Yttrium ද්රාවණයකින් සංසන්දනය කරනු ලැබේ.
2. ප්ලාස්මා ස්කන්ධ වර්ණාවලීක්ෂමිතික (ICP-MS):ICP-MS යනු දියර හා solid න සාම්පලවල යෙට්රීම් අන්තර්ගතය තීරණය කිරීම සඳහා සුදුසු සංවේදී විශ්ලේෂණාත්මක තාක්ෂණයකි. මෙම ක්රමය නියැදිය ආරෝපිත අංශු බවට පරිවර්තනය කර සමූහ විශ්ලේෂණය සඳහා ස්කන්ධ වර්ණාවලීක්ෂයක් භාවිතා කරයි. ICP-MS විසින් පුළුල් ලෙස හඳුනාගැනීමේ පරාසයක් සහ ඉහළ විභේදනයක් ඇති අතර එකවර බහු මූලද්රව්යවල අන්තර්ගතය තීරණය කළ හැකිය. YTTrium හඳුනා ගැනීම සඳහා, ICP-MS ඉතා අඩු හඳුනාගැනීමේ සීමාවන් සහ ඉහළ නිරවද්යතාවයක් ලබා දිය හැකිය.
3. එක්ස් කිරණ ප්රතිදීප්ත දර්ශන වර්ණාවලීක්ෂය (xrf):Xrf යනු solid න හා ද්රව සාම්පලවල YTTrium අන්තර්ගතයන් තීරණය කිරීම සඳහා සුදුසු විනාශකාරී නොවන විශ්ලේෂණ ක්රමයකි. මෙම ක්රමය එක්ස් කිරණ සමඟ සාම්පලයේ මතුපිට ප්රකිරණය සහ නියැදියේ ප්රතිදීප්ත ප්රතිස්ථාපන ප්රතිස්ථාපන ප්රතිනිර්මාණය පිළිබඳ ලක්ෂණ මැනීම මගින් මූලද්රව්ය අන්තර්ගතය තීරණය කරයි. වේගවත් වේගය, සරල ක්රියාකාරිත්වය සහ එකවර බහු මූලද්රව්යයන් තීරණය කිරීමේ හැකියාව එක්සර්ෆ් සතුව ඇත. කෙසේ වෙතත්, අඩු අන්තර්ගත යෙට්රීම් විශ්ලේෂණය කිරීමේදී එක්ස්ආර්එෆ් මැදිහත් විය හැකි අතර එහි ප්රති ing ලයක් ලෙස විශාල දෝෂ ඇති වේ.
4.. ප්රේමණීයව ප්ලාස්මා දෘෂ්ය විමෝචන වර්ණාවලීක්ෂනය (ICP-OES):ප්රේරිත සංක්ෂිප්ත ඔප්ටිකල් විමෝචන වර්ණාවලීක්ෂය බහු මූලද්රව්ය විශ්ලේෂණයේ බහුලව භාවිතා වන ඉතා සංවේදී හා තෝරාගත් විශ්ලේෂණ ක්රමයක් වේ. එය නියැදිය පරමාණුකෘත හා නිශ්චිත තරංග ආයාමය සහ තීව්රතාව මැනීම සඳහා ප්ලාස්මා සාදයිf yttriumවර්ණාවලීක්ෂය විමෝචනය කිරීම. ඉහත ක්රම වලට අමතරව, විද්යුත් රසායනික ක්රමය, වර්ණාවලීක්ෂ භාවිතා කිරීම ආදිය සඳහා YTTrium විසින් හඳුනාගැනීම සඳහා බහුලව භාවිතා වන ක්රම වේ.
YTTRium පරමාණුක අවශෝෂණ ක්රමවේදය
මූලද්රව්ය මැනීම, ප්රේරක මිනුම්, ප්රේරක ජනප්රිය වර්ණාවලීක්ෂමිතික (ICP-MS) යනු ඉතා සංවේදී හා බහු මූලද්රව්ය විශ්ලේෂණ ක්රමවේදයක් වන අතර එය බොහෝ විට භාවිතා කරනුයේ ytrium ඇතුළු මූලද්රව්ය සාන්ද්රණය තීරණය කිරීම සඳහා බොහෝ විට භාවිතා වේ. පහත දැක්වෙන්නේ ICP-MS හි YTTRAM පරීක්ෂා කිරීම සඳහා සවිස්තරාත්මක ක්රියාවලියකි:
1. නියැදි සකස් කිරීම:
නියැදිය සාමාන්යයෙන් ICP-MS විශ්ලේෂණය සඳහා දියර ආකාරයකට විසුරුවා හැරීමට හෝ විසුරුවා හැරිය යුතුය. මෙය රසායනිකව විසුරුවා හැරීම, තාපන ආහාර ජීර්ණය හෝ වෙනත් සුදුසු සැකසුම් ක්රම මගින් කළ හැකිය.
නියැදියට පිළියෙල කිරීම ඕනෑම බාහිර අංගයකින් දූෂණය වීම වැළැක්වීම සඳහා අතිශයින්ම පිරිසිදු කොන්දේසි අවශ්ය වේ. නියැදි අපවිත්ර වීම වළක්වා ගැනීම සඳහා රසායනාගාරය අවශ්ය පියවර ගත යුතුය.
2. ICP පරම්පරාව:
ආගන් හෝ ආගන්-ඔක්සිජන් මිශ්ර ගෑස් සංවෘත ක්වාර්ට්ස්මා පන්දමකට හඳුන්වා දීමෙන් ICP ජනනය වේ. ඉහළ සංඛ්යාත ප්රේරක වර්ණ කප්පාදු කිරීම තීව්ර ප්ලාස්මා ගිනිදැල් නිපදවයි, එය විශ්ලේෂණයේ ආරම්භක ස්ථානය වේ.
ප්ලාස්මා හි උෂ්ණත්වය සෙල්සියස් අංශක 8000 සිට 10000 දක්වා පමණ වන අතර එය නියැදියේ මූලද්රව්ය අයනික තත්වයට පරිවර්තනය කිරීම සඳහා ප්රමාණවත් වන සෙල්සියස් ය.
3. අයනීකරණය සහ වෙන්වීම:නියැදිය ප්ලාස්මාට ඇතුළු වූ පසු, එහි මූලද්රව්ය අයනීකරණය වේ. මෙයින් අදහස් කරන්නේ ඉලෙක්ට්රෝන එකක් හෝ වැඩි ගණනක් අහිමි වන අතර ආරෝපිත අයන සෑදීම. සාමාන්යයෙන් ස්කන්ධ-සිට ආශ්ථ අනුපාතය (M / Z) මගින් විවිධ මූලද්රව්යයන්ගේ අයන වෙන් කිරීම සඳහා ICP-MS ස්කන්ධ වර්ණාවලීක්ෂයක් භාවිතා කරයි. විවිධ මූලද්රව්යයන් වෙන් කොට පසුව විශ්ලේෂණය කිරීම මෙයට මෙයට ඉඩ දෙයි.
4. ස්කන්ධ වර්ණාවලීක්ෂමිතික:වෙන්වූ අයන සමූහ වර්ණාවලියක් ඇතුළත් වේ, සාමාන්යයෙන් චතුරස්රාකාර ස්කන්ධ වර්ණාවලීක්ෂයක් හෝ චුම්බක පරිලෝකනය කිරීමේ ස්කන්ධ වර්ණාවලියක්. ස්කන්ධ වර්ණාවලීක්ෂය තුළ, විවිධ මූලද්රව්යවල අයන වෙන් කර ඔවුන්ගේ සිට ආශ්ථ කිරීමේ අනුපාතය අනුව ඒවා වෙන් කරනු ලැබේ. මෙම අංගය තීරණය කළ යුතු එක් එක් මූලද්රව්යයේ පැමිණ සිටීම හා සාන්ද්රණයට මෙයට ඉඩ දෙයි. ප්ලාස්මා ස්කන්ධ වර්ණාවලීක්ෂමිතික වල එක් වාසියක් එහි ඉහළ යෝජනාවක් වන අතර එමඟින් එකවර විවිධ අංගයන් හඳුනා ගැනීමට එය හැකියාව ලබා දෙයි.
5. දත්ත සැකසීම:ICP-MS විසින් ජනනය කරන ලද දත්ත සාමාන්යයෙන් නියැදියේ මූලද්රව්යවල සාන්ද්රණය තීරණය කිරීම සඳහා ක්රියාවට නංවා විශ්ලේෂණය කළ යුතුය. දන්නා සාන්ද්රණයන්හි ප්රමිතීන්ට අනුව හඳුනාගැනීමේ සං signal ාව සංසන්දනය කිරීම සහ ක්රමාංකනය කිරීම සහ නිවැරදි කිරීම සිදු කිරීම මෙයට ඇතුළත් වේ.
6. ප්රති ult ල වාර්තාව:අවසාන ප්රති result ලය මූලද්රව්යයේ සාන්ද්රණය හෝ ස්කන්ධ ප්රතිශතය ලෙස ඉදිරිපත් කෙරේ. මෙම ප්රති results ල පස් විද්යාව, පාරිසරික විශ්ලේෂණය, ආහාර පරීක්ෂාව, වෛද්ය පර්යේෂණ ආදිය ඇතුළුව විවිධ යෙදුම්වල භාවිතා කළ හැකිය.
ICP-MS යනු yttrium ඇතුළු බහු මූලද්රව්ය විශ්ලේෂණය සඳහා ඉතා නිවැරදි හා සංවේදී තාක්ෂණයක්. කෙසේ වෙතත්, එයට සංකීර්ණ උපකරණ හා විශේෂ ise තාව අවශ්ය වන බැවින් එය සාමාන්යයෙන් රසායනාගාරයක හෝ වෘත්තීය විශ්ලේෂණ මධ්යස්ථානයක සිදු කෙරේ. තථ්ය වැඩ වලදී, වෙබ් අඩවියේ විශේෂිත අවශ්යතා අනුව සුදුසු මිනුම් ක්රමය තෝරා ගැනීම අවශ්ය වේ. රසායනාගාර සහ කර්මාන්තවල YtterBium විශ්ලේෂණය හා හඳුනා ගැනීම සඳහා මෙම ක්රම බහුලව භාවිතා වේ.
ඉහත කරුණු සාරාංශ කිරීමෙන් පසු, YTTRIM අද්විතීය භෞතික හා රසායනික ගුණ සහිත ඉතා රසවත් රසායනික අංගයක් වන අතර එය විද්යාත්මක පර්යේෂණ හා යෙදුම් ක්ෂේත්රවල ඉතා වැදගත් බව අපට නිගමනය කළ හැකිය. ඒ පිළිබඳ අපගේ අවබෝධය තුළ අප යම් ප්රගතියක් ලබා ඇතත්, වැඩිදුර පර්යේෂණ හා ගවේෂණය අවශ්ය වන බොහෝ ප්රශ්න තවමත් තිබේ. අපගේ හැඳින්වීම මගින් පා readers කයන්ට මෙම සිත් ඇදගන්නාසුළු මූලද්රව්යය වඩා හොඳින් තේරුම් ගැනීමට වඩා හොඳින් තේරුම් ගැනීමට උපකාරී වන අතර සෑම කෙනෙකුගේම විද්යාවට හා ගවේෂණය කෙරෙහි උනන්දුවක් දැක්වීමට දිරිගැන්වීමට හේතු වේ යැයි මම බලාපොරොත්තු වෙමි.
වැඩි විස්තර සඳහා Plsඅපව අමතන්නපහත:
ටෙල් සහ WhatS: 008613524231522
Email:Sales@shxlchem.com
පශ්චාත් කාලය: නොවැ. 28-2024