Biliyor musun? İnsanların keşfetme süreciitriyumbükülmeler ve zorluklarla doluydu. 1787'de İsveçli Karl Axel Arrhenius, memleketi Ytterby Köyü yakınındaki bir taş ocağında yanlışlıkla yoğun ve ağır bir siyah cevher keşfetti ve ona "Ytterbite" adını verdi. Bundan sonra, Johan Gadolin, Anders Gustav Ekberg, Friedrich Wöhler ve diğerleri de dahil olmak üzere birçok bilim adamı bu cevher üzerinde derinlemesine araştırma yaptılar.
1794'te Fin kimyager Johan Gadolin, ytterbium cevherinden yeni bir oksit başarıyla ayırdı ve Yttrium adını verdi. İnsanların ilk kez nadir bir toprak unsurunu açıkça keşfettiği idi. Ancak, bu keşif hemen yaygın bir dikkat çekmedi.
Bilim adamları zamanla diğer nadir toprak unsurlarını keşfettiler. 1803'te Alman Klaproth ve İsveçliler Hitzinger ve Berzelius Cerium'u keşfettiler. 1839'da İsveçli Mosander keşfettilantan. 1843'te Erbium'u keşfetti veterbiyum. Bu keşifler, sonraki bilimsel araştırmalar için önemli bir temel sağlamıştır.
Bilim adamları 19. yüzyılın sonuna kadar "yttrium" unsurunu Yttrium cevherinden başarıyla ayırmadı. 1885'te Avusturyalı Wilsbach neodimyum ve praseodomu keşfetti. 1886'da Bois-Baudran keşfettidisporsiyum. Bu keşifler, nadir toprak unsurlarının geniş ailesini daha da zenginleştirdi.
Yttrium'un keşfinden bir asırdan fazla bir süredir, teknik koşulların sınırlamaları nedeniyle, bilim adamları da bazı akademik anlaşmazlıklara ve hatalara neden olan bu unsuru arınamadılar. Ancak bu, bilim adamlarının Yttrium'u inceleme heveslerinden alıkoymadı.
20. yüzyılın başlarında, bilim ve teknolojinin sürekli ilerlemesiyle, bilim adamları nihayet nadir toprak unsurlarını arındırmaya başladılar. 1901'de Fransız Eugene de Marsilya'yı keşfettiEuropyum. 1907-1908'de Avusturyalı Wilsbach ve Fransız Urbain bağımsız olarak lutetium'u keşfetti. Bu keşifler, sonraki bilimsel araştırmalar için önemli bir temel sağlamıştır.
Modern bilim ve teknolojide, Yttrium'un uygulanması gittikçe daha geniş hale geliyor. Bilim ve teknolojinin sürekli ilerlemesiyle, Yttrium'un anlayışımız ve uygulamamız gittikçe daha derinlemesine hale gelecektir.
Yttrium öğesinin uygulama alanları
1.Optik cam ve seramik:Yttrium, esas olarak şeffaf seramik ve optik cam üretiminde optik cam ve seramik üretiminde yaygın olarak kullanılmaktadır. Bileşikleri mükemmel optik özelliklere sahiptir ve lazer, fiber optik iletişim ve diğer ekipman bileşenlerini üretmek için kullanılabilir.
2. Fosforlar:Yttrium bileşikleri fosforlarda önemli bir rol oynar ve parlak floresan yayabilir, bu nedenle genellikle TV ekranları, monitörler ve aydınlatma ekipmanları üretmek için kullanılırlar.Yttrium oksitve diğer bileşikler genellikle ışığın parlaklığını ve netliğini arttırmak için ışıldayan malzemeler olarak kullanılır.
3. Alaşım katkı maddeleri: Metal alaşımlarının üretiminde, yttrium genellikle metallerin mekanik özelliklerini ve korozyon direncini geliştirmek için bir katkı maddesi olarak kullanılır.Yttrium alaşımlarıgenellikle yüksek mukavemetli çelik yapmak için kullanılır vealüminyum alaşımları, onları daha ısıya dayanıklı ve korozyona dayanıklı hale getirir.
4. Katalizörler: Yttrium bileşikleri bazı katalizörlerde önemli bir rol oynar ve kimyasal reaksiyonların hızını hızlandırabilir. Endüstriyel üretim süreçlerinde otomobil egzoz saflaştırma cihazları ve katalizörleri üretmek için kullanılırlar, bu da zararlı maddelerin emisyonunun azaltılmasına yardımcı olur.
5. Tıbbi görüntüleme teknolojisi: Yttrium izotopları, radyofarmasötikleri etiketlemek ve nükleer tıbbi görüntülemenin teşhisi gibi radyoaktif izotoplar hazırlamak için tıbbi görüntüleme teknolojisinde kullanılır.
6. Lazer Teknolojisi:Yttrium iyon lazerleri, çeşitli bilimsel araştırmalarda, lazer tıbbında ve endüstriyel uygulamalarda kullanılan yaygın bir katı hal lazerdir. Bu lazerlerin üretimi, aktivatör olarak belirli yttrium bileşiklerinin kullanılmasını gerektirir.Yttrium öğeleriVe bileşikleri, optik, malzeme bilimi ve tıp gibi birçok alanı içeren modern bilim ve teknoloji ve endüstride önemli bir rol oynamaktadır ve insan toplumunun ilerlemesine ve gelişimine olumlu katkılarda bulunmuştur.
Yttrium'un fiziksel özellikleri
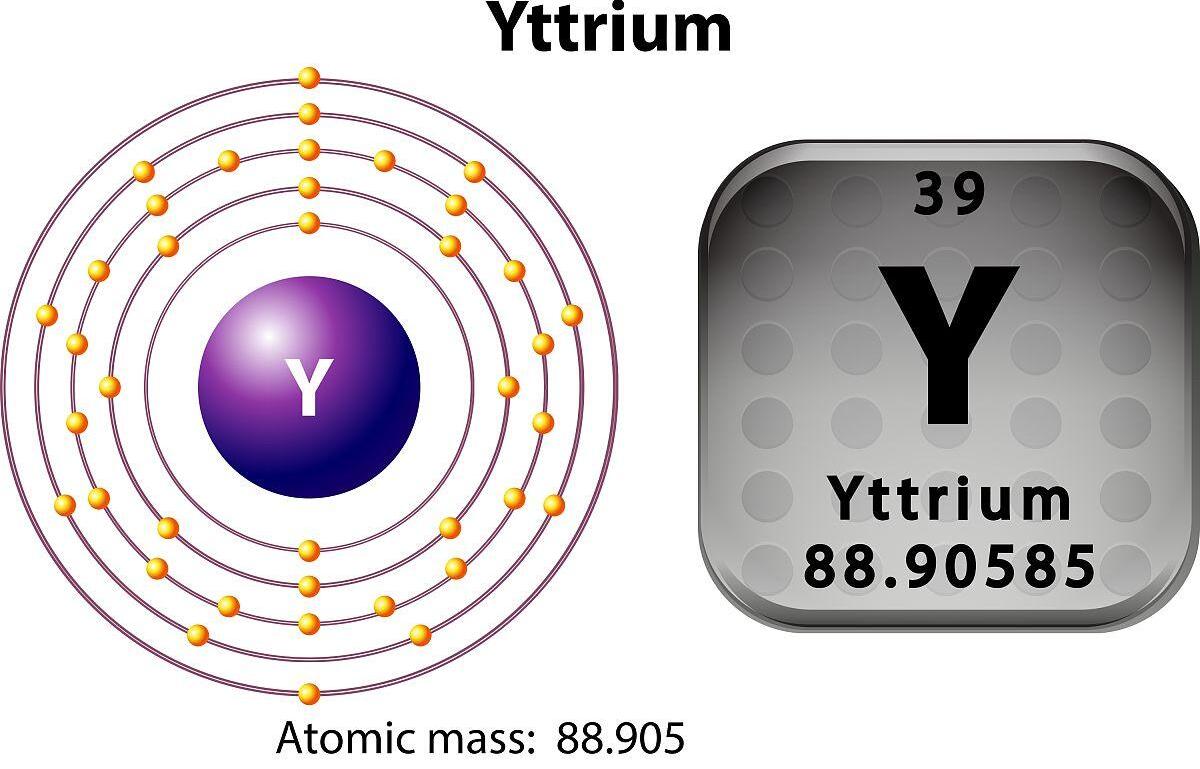
Atom sayısıitriyum39 ve kimyasal sembolü Y'dir.
1. Görünüm:Yttrium gümüş-beyaz bir metaldir.
2. Yoğunluk:Yttrium yoğunluğu 4.47 g/cm3'tür, bu da onu Dünya kabuğundaki nispeten ağır elementlerden biri yapar.
3. Erime noktası:Yttrium'un erime noktası 1522 santigrat derecedir (2782 derece Fahrenheit), bu da yttrium'un termal koşullar altında bir katıdan bir sıvıya değiştiği sıcaklığı ifade eder.
4. Kaynama noktası:Yttrium'un kaynama noktası 3336 santigrat derecedir (6037 derece Fahrenheit), bu da yttrium'un bir sıvıdan bir gaza termal koşullar altında değiştiği sıcaklığı ifade eder.
5. Aşama:Oda sıcaklığında, yttrium sağlam bir haldedir.
6. İletkenlik:Yttrium, yüksek iletkenliğe sahip iyi bir elektrik iletkenidir, bu nedenle elektronik cihaz üretimi ve devre teknolojisinde belirli uygulamalara sahiptir.
7. Magnetizma:Yttrium, oda sıcaklığında paramanyetik bir malzemedir, yani manyetik alanlara belirgin bir manyetik tepkiye sahip değildir.
8. Kristal Yapı: Yttrium altıgen yakın paketlenmiş bir kristal yapıda bulunur.
9. Atom hacmi:Yttrium'un atom hacmi, bir mol yttrium atomunun işgal ettiği hacmi ifade eden mol başına 19.8 santimetredir.
Yttrium, nispeten yüksek yoğunluk ve erime noktasına sahip metalik bir elementtir ve iletkenliğe iyi sahiptir, bu nedenle elektronik, malzeme bilimi ve diğer alanlarda önemli uygulamalara sahiptir. Aynı zamanda, Yttrium aynı zamanda bazı ileri teknolojilerde ve endüstriyel uygulamalarda önemli bir rol oynayan nispeten yaygın bir nadir unsurdur.
Yttrium'un kimyasal özellikleri
1. Kimyasal sembol ve grup: Yttrium'un kimyasal sembolü y'dir ve periyodik tablonun beşinci döneminde, lantanid elemanlarına benzer üçüncü grup bulunur.
2. Elektronik Yapı: Yttrium'un elektronik yapısı 1S² 2S² 2P⁶ 3S² 3P⁶ 3D⁰ 4S² 4P⁶ 4D⁰ 4F⁴ 5S²'dir. Dış elektron tabakasında, Yttrium'un iki değerlik elektronu vardır.
3. Valans Durumu: Yttrium genellikle en yaygın değerlik durumu olan +3'ün bir değerlik durumu gösterir, ancak +2 ve +1 değerlik durumlarını da gösterebilir.
4. Reaktivite: Yttrium nispeten kararlı bir metaldir, ancak havaya maruz kaldığında yavaş yavaş oksitlenir ve yüzeyde bir oksit tabakası oluşturur. Bu, Yttrium'un parlaklığını kaybetmesine neden olur. Yttrium'u korumak için genellikle kuru bir ortamda saklanır.
5. Oksitlerle reaksiyon: Yttrium, çeşitli bileşikler oluşturmak için oksitlerle reaksiyona girer,yttrium oksit(Y2O3). Yttrium oksit genellikle fosfor ve seramik yapmak için kullanılır.
6. ** Asitlerle reaksiyon **: Yttrium, karşılık gelen tuzları üretmek için güçlü asitlerle tepki verebilir, örneğinyttrium klorür (YCL3) veyayttrium sülfat (Y2 (SO4) 3).
7. Su ile reaksiyon: Yttrium, normal koşullar altında doğrudan su ile reaksiyona girmez, ancak yüksek sıcaklıklarda, hidrojen ve yttrium oksit üretmek için su buharı ile reaksiyona girebilir.
8. Sülfitler ve karbürler ile reaksiyon: Yttrium, yttrium sülfür (YS) ve Yttrium karbür (YC2) gibi karşılık gelen bileşikler oluşturmak için sülfitler ve karbürlerle reaksiyona girebilir. 9. İzotoplar: Yttrium, en istikrarlı olanı, uzun bir yarı ömrü olan ve nükleer tıp ve izotop etiketlemesinde kullanılan yttrium-89 (^89y) olan çoklu izotoplara sahiptir.
Yttrium, çoklu değerlik durumlarına sahip nispeten kararlı bir metalik elementtir ve bileşikler oluşturmak için diğer elementlerle reaksiyona girme yeteneğidir. Optik, malzeme bilimi, tıp ve endüstride, özellikle fosfor, seramik üretim ve lazer teknolojisinde çok çeşitli uygulamalara sahiptir.
Yttrium'un biyolojik özellikleri
Biyolojik özellikleriitriyumCanlı organizmalarda nispeten sınırlıdır.
1. Varlık ve yutma: Yttrium yaşam için gerekli bir unsur olmasa da, toprak, kayalar ve su da dahil olmak üzere doğada eser miktarda yttrium bulunabilir. Organizmalar, genellikle toprak ve bitkilerden, gıda zincirinden eser miktarda yttrium yutabilir.
2. Biyoyararlanım: Yttrium'un biyoyararlanımı nispeten düşüktür, bu da organizmaların genellikle yttrium'u etkili bir şekilde emmek ve kullanmakta güçlük çektiği anlamına gelir. Çoğu yttrium bileşiği organizmalarda kolayca emilmez, bu nedenle atılma eğilimindedirler.
3. Organizmalarda dağılım: Bir organizma içinde, yttrium esas olarak karaciğer, böbrek, dalak, akciğerler ve kemikler gibi dokulara dağıtılır. Özellikle, kemikler daha yüksek konsantrasyonlarda yttrium içerir.
4. Metabolizma ve atılım: Yttrium'un insan vücudundaki metabolizması nispeten sınırlıdır, çünkü organizmayı genellikle atılım yoluyla bırakır. Çoğu idrardan atılır ve dışkılama şeklinde de atılabilir.
5. Toksisite: Düşük biyoyararlanımı nedeniyle, Yttrium genellikle normal organizmalarda zararlı seviyelere birikmez. Bununla birlikte, yüksek doz yttriyum maruziyetinin organizmalar üzerinde zararlı etkileri olabilir ve bu da toksik etkilere yol açabilir. Bu durum genellikle nadiren ortaya çıkar, çünkü doğadaki yttriyum konsantrasyonları genellikle düşüktür ve organizmalara yaygın olarak kullanılmaz veya maruz kalmaz. Organizmalarda yttrium'un biyolojik özellikleri esas olarak eser miktarlarda, düşük biyoyararlanım ve yaşam için gerekli bir element olmasıyla ortaya çıkar. Normal koşullar altında organizmalar üzerinde belirgin toksik etkileri olmasa da, yüksek doz yttriyum maruziyeti sağlık tehlikelerine neden olabilir. Bu nedenle, bilimsel araştırma ve izleme, Yttrium'un güvenliği ve biyolojik etkileri için hala önemlidir.
Yttrium'un doğada dağılımı
Yttrium, saf temel formda olmasa da, doğada nispeten yaygın olarak dağıtılan nadir bir toprak elemanıdır.
1. Dünya kabuğunda meydana gelme: Yttrium'un Dünya kabuğundaki bolluğu nispeten düşüktür ve ortalama 33 mg/kg konsantrasyonu ile. Bu, Yttrium'u nadir unsurlardan biri yapar.
Yttrium esas olarak mineraller şeklinde, genellikle diğer nadir toprak elemanlarıyla birlikte bulunur. Bazı büyük yttrium mineralleri arasında yttrium demir garnet (yig) ve yttrium oksalat (y2 (C2O4) 3) bulunur.
2. Coğrafi Dağılım: Yttrium yatakları tüm dünyaya dağıtılır, ancak bazı alanlar yttrium açısından zengin olabilir. Bazı büyük yttrium yatakları aşağıdaki bölgelerde bulunabilir: Avustralya, Çin, Amerika Birleşik Devletleri, Rusya, Kanada, Hindistan, İskandinavya, vb. 3. Çıkarma ve İşleme: Yttrium cevheri çıkarıldıktan sonra, kimyasal işleme genellikle yttriumu çıkarmak ve ayırmak için gereklidir. Bu genellikle yüksek saflıkta yttrium elde etmek için asit sızıntısı ve kimyasal ayırma işlemlerini içerir.
Yttrium gibi nadir toprak elemanlarının genellikle saf elementler şeklinde bulunmadığını, ancak diğer nadir toprak elemanlarıyla karıştırıldığını belirtmek önemlidir. Bu nedenle, daha yüksek saflıkta yttrium ekstraksiyonu karmaşık kimyasal işleme ve ayırma işlemleri gerektirir. Ayrıca, arzıNadir toprak unsurlarıSınırlıdır, bu nedenle kaynak yönetimi ve çevresel sürdürülebilirliklerinin dikkate alınması da önemlidir.
Yttrium elementinin madencilik, çıkarılması ve eritmesi
Yttrium, genellikle saf yttrium şeklinde değil, yttrium cevheri şeklinde var olan nadir bir toprak elemanıdır. Aşağıda, yttrium elementinin madencilik ve rafine sürecine ayrıntılı bir giriş:
1. Yttrium cevherinin madenciliği:
Keşif: Birincisi, jeologlar ve madencilik mühendisleri, yttrium içeren mevduat bulmak için keşif çalışmaları yürütmektedir. Bu genellikle jeolojik çalışmalar, jeofizik keşif ve örnek analizini içerir. Madencilik: Yttrium içeren bir depozito bulunduktan sonra cevher çıkarılır. Bu birikintiler genellikle yttrium demir garnet (yig) veya yttrium oksalat (y2 (C2O4) 3) gibi oksit cevherleri içerir. Cevher Kırma: Madencilikten sonra, cevherin genellikle sonraki işlem için daha küçük parçalara ayrılması gerekir.
2. Yttrium'u çıkarma:Kimyasal liç: Ezilmiş cevher genellikle bir izabe tesisine gönderilir, burada yttrium kimyasal liç yoluyla çıkarılır. Bu işlem genellikle yttriyumu cevherden çözmek için sülfürik asit gibi asidik bir sızıntı çözeltisi kullanır. Ayrılık: Yttrium çözüldükten sonra, genellikle diğer nadir toprak elemanları ve safsızlıkları ile karıştırılır. Daha yüksek saflıkta yttrium çıkarmak için, genellikle solvent ekstraksiyonu, iyon değişimi veya diğer kimyasal yöntemler kullanılarak bir ayırma işlemi gereklidir. Yağış: Yttrium, saf yttrium bileşikleri oluşturmak için uygun kimyasal reaksiyonlar yoluyla diğer nadir toprak elemanlarından ayrılır. Kurutma ve Kalsinasyon: Elde edilen yttriyum bileşiklerinin genellikle nihayetinde saf yttrium metal veya bileşikler elde etmek için kalıntı nem ve safsızlıkları uzaklaştırmak için kurutulması ve kalsine edilmesi gerekir.
Yttrium'un algılama yöntemleri
Yttrium için yaygın tespit yöntemleri esas olarak atomik absorpsiyon spektroskopisi (AAS), endüktif olarak bağlanmış plazma kütle spektrometrisi (ICP-MS), X-ışını floresan spektroskopisi (XRF), vb.
1. Atomik absorpsiyon spektroskopisi (AAS):AAS, çözeltideki yttrium içeriğinin belirlenmesi için uygun yaygın olarak kullanılan bir nicel analiz yöntemidir. Bu yöntem, numunedeki hedef eleman belirli bir dalga boyunun ışığını emdiğinde emilim fenomenine dayanır. İlk olarak, numune, gaz yanması ve yüksek sıcaklık kurutma gibi ön tedavi aşamalarıyla ölçülebilir bir forma dönüştürülür. Daha sonra, hedef elemanın dalga boyuna karşılık gelen ışık numuneye geçirilir, numune tarafından emilen ışık yoğunluğu ölçülür ve numunedeki yttrium içeriği, bilinen bir konsantrasyonun standart bir yttrium çözeltisi ile karşılaştırılarak hesaplanır.
2. Endüktif olarak bağlanmış plazma kütle spektrometrisi (ICP-MS):ICP-MS, sıvı ve katı numunelerdeki yttrium içeriğinin belirlenmesi için uygun oldukça hassas bir analitik tekniktir. Bu yöntem numuneyi yüklü parçacıklara dönüştürür ve daha sonra kütle analizi için bir kütle spektrometresi kullanır. ICP-MS geniş bir algılama aralığına ve yüksek çözünürlüğe sahiptir ve aynı anda birden fazla öğenin içeriğini belirleyebilir. Yttrium tespiti için ICP-MS çok düşük algılama sınırları ve yüksek doğruluk sağlayabilir.
3. X-ışını floresan spektrometrisi (XRF):XRF, katı ve sıvı numunelerde yttrium içeriğinin belirlenmesi için uygun tahribatsız bir analitik yöntemdir. Bu yöntem, numunenin yüzeyini X-ışınları ile ışınlayarak ve numunedeki floresan spektrumunun karakteristik tepe yoğunluğunu ölçerek eleman içeriğini belirler. XRF, hızlı hız, basit çalışma ve aynı anda birden fazla öğeyi belirleme yeteneğine sahiptir. Bununla birlikte, XRF, düşük içerikli yttrium analizine müdahale edilebilir ve bu da büyük hatalara neden olabilir.
4. Endüktif olarak bağlanmış plazma optik emisyon spektrometrisi (ICP-OES):Endüktif olarak bağlanmış plazma optik emisyon spektrometrisi, çok elemanlı analizde yaygın olarak kullanılan oldukça hassas ve seçici bir analitik yöntemdir. Örneği atomize eder ve spesifik dalga boyunu ve yoğunluğunu ölçmek için bir plazma oluştururf yttriumSpektrometrede emisyon. Yukarıdaki yöntemlere ek olarak, elektrokimyasal yöntem, spektrofotometri, vb. Dahil olmak üzere yttrium tespiti için yaygın olarak kullanılan diğer yöntemler de vardır. Uygun bir algılama yönteminin seçimi, örnek özellikleri, gerekli ölçüm aralığı ve tespit doğruluğu ve kalibrasyon standartları gibi faktörlere bağlıdır.
Yttrium atomik absorpsiyon yönteminin spesifik uygulaması
Eleman ölçümünde, endüktif olarak birleştirilmiş plazma kütle spektrometresi (ICP-MS), genellikle yttrium dahil elementlerin konsantrasyonunu belirlemek için kullanılan oldukça hassas ve çok elemanlı bir analiz tekniğidir. Aşağıda ICP-MS'de yttrium'u test etmek için ayrıntılı bir süreç:
1. Örnek hazırlama:
Numunenin genellikle ICP-MS analizi için çözülmesi veya sıvı bir forma dönüştürülmesi gerekir. Bu, kimyasal çözünme, ısıtma sindirimi veya diğer uygun hazırlık yöntemleri ile yapılabilir.
Numunenin hazırlanması, herhangi bir dış eleman tarafından kontaminasyonu önlemek için son derece temiz koşullar gerektirir. Laboratuvar numune kontaminasyonunu önlemek için gerekli önlemleri almalıdır.
2. ICP Üretimi:
ICP, kapalı bir kuvars plazma meşalesine argon veya argon-oksijen karışık gaz eklenerek üretilir. Yüksek frekanslı endüktif kuplaj, analizin başlangıç noktası olan yoğun bir plazma alevi üretir.
Plazmanın sıcaklığı, numunedeki elementleri iyonik duruma dönüştürecek kadar yüksek olan yaklaşık 8000 ila 10000 santigrat derecedir.
3. İyonizasyon ve Ayırma:Örnek plazmaya girdikten sonra, içindeki elemanlar iyonize edilir. Bu, atomların bir veya daha fazla elektron kaybettiği ve yüklü iyonlar oluşturduğu anlamına gelir. ICP-MS, farklı elementlerin iyonlarını, genellikle kütle-şarj oranına (m/z) ayırmak için bir kütle spektrometresi kullanır. Bu, farklı elementlerin iyonlarının ayrılmasını ve daha sonra analiz edilmesini sağlar.
4 Kütle spektrometrisi:Ayrılan iyonlar bir kütle spektrometresi, genellikle bir dörtlü kütle spektrometresi veya manyetik bir tarama kütle spektrometresi girer. Kütle spektrometresinde, farklı elementlerin iyonları ayrılır ve kütle-şarj oranlarına göre tespit edilir. Bu, her elemanın varlığının ve konsantrasyonunun belirlenmesini sağlar. Endüktif olarak bağlanmış plazma kütle spektrometrisinin avantajlarından biri, yüksek çözünürlüğüdür, bu da birden fazla elemanı aynı anda tespit etmesini sağlar.
5. Veri İşleme:ICP-MS tarafından üretilen verilerin genellikle numunedeki elemanların konsantrasyonunu belirlemek için işlenmesi ve analiz edilmesi gerekir. Bu, algılama sinyalinin bilinen konsantrasyon standartları ile karşılaştırılmasını ve kalibrasyon ve düzeltme yapmayı içerir.
6. Sonuç Raporu:Nihai sonuç, elemanın konsantrasyonu veya kütle yüzdesi olarak sunulmaktadır. Bu sonuçlar, Dünya Bilimi, Çevresel Analiz, Gıda Testi, Tıbbi Araştırma vb. Gibi çeşitli uygulamalarda kullanılabilir.
ICP-MS, Yttrium da dahil olmak üzere çok elemanlı analiz için uygun son derece doğru ve hassas bir tekniktir. Bununla birlikte, karmaşık enstrümantasyon ve uzmanlık gerektirir, bu nedenle genellikle bir laboratuvarda veya profesyonel bir analiz merkezinde gerçekleştirilir. Gerçek çalışmada, sitenin özel ihtiyaçlarına göre uygun ölçüm yöntemini seçmek gerekir. Bu yöntemler laboratuvarlarda ve endüstrilerde ytterbium analizi ve tespitinde yaygın olarak kullanılmaktadır.
Yukarıdakileri özetledikten sonra, Yttrium'un bilimsel araştırma ve uygulama alanlarında büyük önem taşıyan benzersiz fiziksel ve kimyasal özelliklere sahip çok ilginç bir kimyasal unsur olduğu sonucuna varabiliriz. Her ne kadar bunu anlamamızda biraz ilerleme kaydetmiş olsak da, daha fazla araştırma ve keşif gerektiren birçok soru var. Umarım tanıtımımız okuyucuların bu büyüleyici unsuru daha iyi anlamalarına yardımcı olabilir ve herkesin bilime ve keşiflere olan ilgisine ilham verebilir.
Daha fazla bilgi için lütfenbize Ulaşınaltında:
Tel & Whats: 008613524231522
Email:Sales@shxlchem.com
Gönderme Zamanı:-28-2024 Kasım