Wisten jo dat? It proses fan it ûntdekken fan minskenYttriumwie fol mei twisten en útdagings. Yn 1787 ûntduts de Swede Karl Axel per ongelok in ticht en swier swart-erts yn in steengroeven by syn berteplak fan Ytterby doarp en neamde it "Ytterbite". Hjirnei ynklusyf in protte wittenskippers, ynklusyf Johan Gadolin, Anders Gustav Ekberg, Friedrich Wöhler en oaren fierden yngeande yn-djipte ûndersyk op dizze erts.
Yn 1794 skieden Finnish chemist Johan Gadolin mei súkses in nije okside fan Ytterbium Ore en neamde it Yttrium. Dit wie de earste kear dat minsken dúdlik in seldsume ierdeelemint ûntdutsen. Dizze ûntdekking liet lykwols lykwols net wiidweidich oansprekke
Oer de tiid hawwe wittenskippers oare seldsume ierde-eleminten ûntdutsen. Yn 1803, it Dútske Klaproth en de Sweden Hitzinger en Berzelius ûntdutsen Cerium. Yn 1839 ûntduts de Swede MoanderLanthanum. Yn 1843 ûntduts hy erbium enterbium. Dizze ûntdekkingen levere in wichtige stifting foar folgjende wittenskiplik ûndersyk.
It wie net oant it ein fan 'e 19e iuw dat wittenskippers it elemint "Yttrium" mei súkses skieden fan Yttrium Ore. Yn 1885 ûntduts Eastenrykske Wilsbach Neodymium en PrasodyMium. Yn 1886 ûntduts Bois-Baudrandysprosium. Dizze ûntdekkingen ferryke fierder de grutte famylje fan seldsume ierde-eleminten.
Foar mear as in ieu nei de ûntdekking fan Yttrium, fanwegen de beheiningen fan technyske omstannichheden kinne wittenskippers dit elemint net suvere, dy't ek wat akademyske skeel en flaters hawwe feroarsake. Dit stoppe lykwols gjin wittenskippers út har entûsjasme foar it studearjen fan Yttrium.
Yn 'e iere 20e iuw, mei it trochgeande foarútgong fan wittenskip en technology, begon wittenskippers einlings om seldsume ierde-eleminten te reinigjen. Yn 1901, Frânsman Eugene De Marseille ûntdutseuropium. Yn 1907-1908, Eastenrykske Wilsbach en Frânsman Urbain ûntdekte selsstannich Lutetium. Dizze ûntdekkingen levere in wichtige stifting foar folgjende wittenskiplik ûndersyk.
Yn moderne wittenskip en technology wurdt de tapassing fan Yttrium mear en wiidweidich wurden. Mei it trochgeande foarútgong fan wittenskip en technology sil ús begryp en tapassing fan Yttrium mear en mear yngeande wurde.
Oanfraachfjilden fan Yttrium Element
1.Optysk glês en keramyk:Yttrium wurdt breed brûkt yn 'e fabrikaazje fan optysk glês en keramyk, fral yn' e fabrikaazje yn 'e fabrikaazje fan transparante keramyk en optysk glês. De ferbiningen hawwe poerbêste optyske eigenskippen en kinne brûkt wurde om komponinten fan lasers te produsearjen, glêstried-optyske kommunikaasje en oare apparatuer.
2 Foshors:Yttrium-ferbiningen spielje in wichtige rol yn fosfor en kinne ljochte fluoresce emitearje, sadat se faak wurde brûkt om troch te produsearjen om de skriklike skermen te produsearjen, monitoren en ferljochtingapparatuer.Yttrium OxideEn oare ferbiningen wurde faak brûkt as lúzend materialen om de helderheid en dúdlikens fan ljocht te ferbetterjen.
3 Toilingen fan Alloy: Yn 'e produksje fan metalen alloys wurdt Yttrium faak brûkt as addatyf om de meganyske eigenskippen en korroenresresjering fan metalen te ferbetterjen.Yttrium Alloyswurde faak brûkt om stiel mei hege sterkte te meitsjen enAluminium Alloys, wêrtroch se mear hjittebestindich en korrosysjebestindich binne.
4. Katalyssts: Yttrium-ferbiningen spielje in wichtige rol yn guon katalysinten en kin it taryf fan gemyske reaksjes fersnelle. Se wurde brûkt om auto-útlaatfersifikker en katalysjen yn yndustriële produksjeprosessen te produsearjen, te helpen om de emisje fan skealike stoffen te ferminderjen.
5. Medyske ferbyldingstechnology: Yttrium Isotopen wurde brûkt yn medyske ferbyldingstechnology om radioaktive isotopen te tarieden, lykas foar etikette fan radiofarreteare nukleêre medyske imaging.
6. Laser Technology:Yttrium Io-lasers binne in mienskiplike steatssteat Laser brûkt yn ferskate wittenskiplik ûndersyk, laser medisyn en yndustriële applikaasjes. De fabrikaazje fan dizze lasers fereasket it gebrûk fan bepaalde Yttrium-ferbiningen as aktivators.Yttrium elemintenEn har ferbiningen spielje in wichtige rol yn moderne wittenskip en de technyk, wêrtroch in protte fjilden binne, lykas optyk, materialen wittenskip, en medisinen en medisinen makke ta de foarútgong en ûntwikkeling fan 'e minske maatskippij.
Fysike eigenskippen fan Yttrium
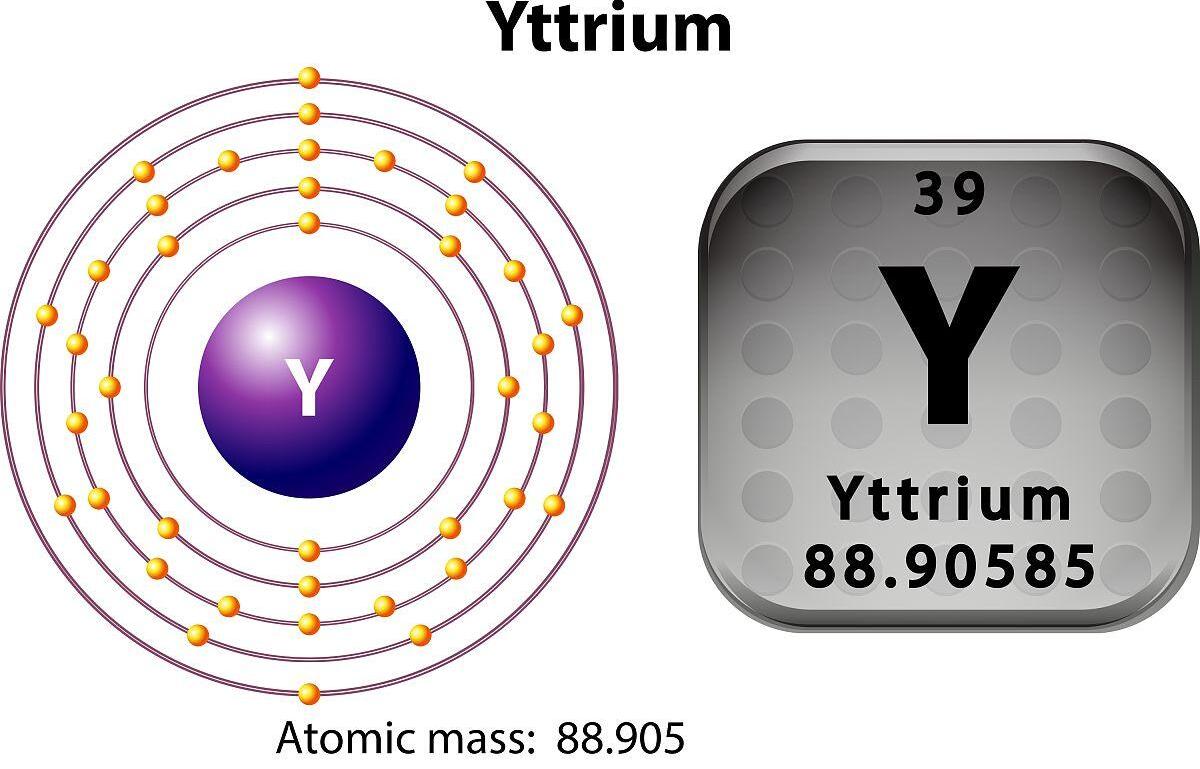
It atoomnûmer fanYttriumis 39 en it gemysk symboal is Y.
1 Beskriuwing:Yttrium is in sulveren-wyt metaal.
2. DENSITY:De tichtheid fan ITRUM is 4.47 G / CM3, wat makket it ien fan 'e relatyf swiere eleminten yn' e ierdkorst.
3. Melting point:It smeltpunt fan Yttrium is 1522 graden Celsius (2782 graden Fahrenheit), dy't ferwiist nei de temperatuer wêrop Yttrium feroaret fan in solide nei in floeistof ûnder thermyske omstannichheden.
4. Siwiling punt:It siedpunt fan Yttrium is 3336 graden Celsius (6037 graden Fahrenheit), dy't ferwiist nei de temperatuer wêrop Yttrium feroaret fan in floeistof nei in gas ûnder thermyske omstannichheden.
5 Fase:By keamertemperatuer is yttrium yn in solide steat.
6 Direkt.Yttrium is in goede konduktor fan elektrisiteit mei hege gedrach, dus it hat bepaalde applikaasjes yn elektroanyske apparaat-fabrikaazje en circuittechnology.
7 Magnetisme:Yttrium is in paramagnetysk materiaal by keamertemperatuer, wat betsjut dat it net foar de hân lizzende magnetyske reaksje op magnetyske fjilden hat.
8 Crystal Structure: Yttrium bestiet yn in hexagonale tichtby ynpakt kristalstruktuer.
9. Atoomvolume:It atoomvumum fan Yttrium is 19.8 kubike sintimeter per mole, dy't ferwiist nei it folume beset troch ien mol fan Yttrium atomen.
Yttrium is in metalen elemint mei relatyf hege tichtheid en smeltpunt, en hat goede konduktiviteit, dus it hat wichtige applikaasjes yn elektroanika, materialen wittenskip en oare fjilden. Tagelyk is Yttrium ek in relatyf mienskiplik seldsume elemint, dy't in wichtige rol spilet yn guon avansearre technologyen en yndustriële applikaasjes.
Gemyske eigenskippen fan Yttrium
1. Gemyske symboal en groep: it gemyske symboal fan Yttrium is y, en it leit yn 'e fyfde perioade fan' e periodike tabel, de tredde groep, dy't gelyk is oan 'e Lanthanide-eleminten.
2 Electronic Struktuer: De elektroanyske struktuer fan Yttrium is 1S² 2S² 2P⁶ 3S² 3P⁶ 3D¹⁰ 4S² 4P⁶ 4D¹⁰ 4F¹⁴ 5S². Yn 'e Outer Electra-laach hat Yttrium twa Valence-elektroanen.
3. VALENCE STAT: Yttrium toant normaal in Valens State of +3, dat is de meast foarkommende steat, mar it kin ek Valenteaten sjen litte fan +2 en +1.
4. Reaktiviteit: Yttrium is in relatyf stabylmetaal, mar it sil stadichoan oksidisearje as se bleatsteld binne oan loft, foarmje in okside laach op it oerflak. Dit feroarsaket Yttrium syn glâns te ferliezen. Om Yttrium te beskermjen, wurdt it normaal opslein yn in droege omjouwing.
5. REAKSJE MEI OSIDES: YTTRIUM reaksjes reageart mei oksides om ferskate ferbiningen te foarmjen, ynklusyfYttrium Oxide(Y2o3. Yttrium Oxide wurdt faak brûkt om fosforen en keramyk te meitsjen.
6 ** REAKSJE MET ECIDS **: Yttrium kin reagearje mei sterke soeren om korrespondearjende sâlt te produsearjen, lykasYttrium-chloride (YCL3) ofYttrium Sulfate (Y2 (SO4) 3).
7 Reaksje mei wetter: Yttrium reageart net direkt mei wetter ûnder normale omstannichheden, mar by hege temperatueren, kin it reagearje mei wetterdamp om hydrogen te produsearjen om hydrogen te produsearjen en yllúten
8 reaksje mei sullauwe en karien: Yttrium kinne reagearje mei sulfides en karbanen om korrespondearjende ferbiningen te foarmjen lykas YTTrium Sulfide (YS) en YTTrium Carbide (YC2). 9. Isotopes: ITTrium hat meardere isotopen, de meast stabile dêrfan is Yttrium-89 (^ 89y), dy't in lang heal libben hat en wurdt brûkt yn nukleêre medisinen en isotopet etikettering.
Yttrium is in relatyf stabyl Metaal elemint mei meardere valens steaten en de mooglikheid om te reagearjen mei oare eleminten om ferbiningen te foarmjen. It hat in breed oanbod fan applikaasjes yn optyk, materialen wittenskip, medisinen, en sektor, foaral yn fosfor, keramyske fabrikaazje, en lasertechnology.
Biologyske eigenskippen fan Yttrium
De biologyske eigenskippen fanYttriumyn libbene organismen binne relatyf beheind.
1. Oanwêzigens en opname: Hoewol Yttrium net in elemint is om it libben net in elemint is, tracebedrach fan Yttrium kinne fûn wurde yn 'e natuer, ynklusyf grûn, rotsen, rotsen, en wetter. Organismen kinne spoaren yntsjinje fan Yttrium troch de fiedselketen, meast fan boaiem en planten.
2. Bioavesberens: De Bioavaanberens fan Yttrium is relatyf leech, wat betsjut dat organismen yn 't algemien problemen hawwe om Yttrium effektyf te absorbearjen en te brûken. De measte Yttrium-ferbiningen wurde net maklik opnommen yn organismen, sadat se tendearje te wurde útsteld.
3. Distribution in organisms: Once in an organism, yttrium is mainly distributed in tissues such as the liver, kidney, spleen, lungs, and bones. Benammen befetsje bonken hegere konsintraasjes fan Yttrium.
4. Metabolisme en ekskresje: It metabolisme fan Yttrium yn it minsklik lichem is relatyf beheind, om't it normaal it organisme wurdt ferlit troch ekskresje. De measte dêrfan wurdt útsteld troch urine, en it kin ek útsteld wurde yn 'e foarm fan defekaasje.
5. Toxicity: Fanwegen syn lege Bio-bioavailabiliteit sammelt Yttrium net normaal oan skealike nivo's yn normale organismen. Lykwols, high-dosis-eksposysje lykwols kin skealike effekten hawwe op organismen, dy't liede ta toxyske effekten. Dizze situaasje bart normaal, om't Yttrium konsintraasjes normaal leech binne en it is net breed brûkt as biologyske skaaimerken fan Yttrium yn 'e oanwêzigens yn' e oanwêzigens yn 'e oanwêzigens, en net in elemint nedich foar it libben. Hoewol it net foar de hân lizzende giftige effekten hat ûnder organismen ûnder normale omstannichheden, kin de eksposysje fan High-doaze kinne feroarsaakje sûnens gefaren feroarsaakje. Dêrom binne wittenskiplik ûndersyk en monitoaring noch wichtich foar de feiligens en biologyske effekten fan Yttrium.
Distribúsje fan Yttrium yn 'e natuer
Yttrium is in seldsume ierde-elemint dat relatyf breed ferdield is yn 'e natuer, hoewol it net bestiet yn pure elementale foarm.
1. Foarkommen yn 'e ierdkoarne: de oerfloed fan Yttrium yn' e ierde fan 'e ierde is relatyf leech, mei in gemiddelde konsintraasje fan sawat 33 mg / kg. Dit makket Yttrium ien fan 'e seldsume eleminten.
Yttrium bestiet foaral yn 'e foarm fan mineralen, meastentiids tegearre mei oare seldsume ierde eleminten. Guon grutte Yttrium-mineralen omfetsje Yttrium Iron Iron-Garnet (Yig) en Yttrium Oxalate (Y2 (C2O4) 3).
2. Geografyske ferdieling: Yttrium-ôfsettings wurde oer de heule wrâld ferspraat, mar guon gebieten kinne ryk wêze yn Yttrium. Guon Major Yttrium-ôfsettings kinne fûn wurde yn 'e folgjende regio's: Austraalje, Sina, Feriene Steaten, Kanada, EXTRIMAVIA (EXCTRIUM EN DE YTTRIUM EN CHEMISCHE FERGESE PROLEMPEN WURDT FERGESE OM DE YTTRIUM. Dit omfettet normaal soere leden en gemyske skiedingsprosessen om High-Purity Yttrium te krijen.
It is wichtich om te merken dat seldsume ierde-eleminten binne, lykas Yttrium net normaal besteane yn 'e foarm fan suvere eleminten, mar wurde mongen mei oare seldsume ierde-eleminten. Dêrom fereasket de ekstraksje fan hegere suverheid Yttrium kompleks gemyske ferwurking en skiedingsprosessen. Derneist, it oanbod fanseldsume ierde elemintenis beheind, sadat beskôging fan har boarnebehear en miljeu duorsumens is ek wichtich.
Mynbou, ekstraksje en smelten fan Yttrium-elemint
Yttrium is in seldsume ierde elemint dat normaal bestiet yn 'e foarm fan pure Yttrium, mar yn' e foarm fan Yttrium Ore. It folgjende is in detaillearre ynlieding op it mining en ferfine proses fan Yttrium-elemint:
1 Mining fan Yttrium Ore:
Ferkenning: Earste, geologen en in mining yngenieurs útfiere ferkenningwurk om ôfsettings te finen dy't Yttrium befetsje. Dit omfettet normaal geologyske stúdzjes, geofysyske ferkenning, en foarbyldnanalyse. MINING: Ienris is in boarch befette Yttrium fûn, wurdt de ore min. Dizze ôfsettings omfetsje normaal oxide-eares lykas Yttrium Iron-Garnet (Yig) of Yttrium Oxalate (Y2 (C2O4) 3). Ore ferplettering: Nei myning moat de ore normaal wurde brutsen yn lytsere stikken foar folgjende ferwurking.
2 EXTRACTING YTTRIUM:Gemyske lacht: de kreaze ore wurdt normaal stjoerd nei in smelter, wêr't Yttrium wurdt ekstrahearre troch gemyske leugend. Dit proses brûkt normaal in soere leugend oplossing, lykas sulfuryske soer, om it Yttrium fan 'e Ore te lossen. Skieding: Ienris wurdt Yttrium ûntbûn, wurdt it normaal mingd mei oare seldsume ierde-eleminten en ûnreinheden. Om Yttrium fan hegere suverens te ekstrahearjen is in skiedingsproses ferplicht, normaal gebrûk fan solvent-ekstraksje, ion útwikseling as oare gemyske metoaden. Neerslach: Yttrium wurdt skieden fan oare seldsume ierde-eleminten fia passende gemyske reaksjes om pure Yttrium-ferbiningen te foarmjen. Droegjen en kalsy: De behelle Yttrium-ferbiningen moatte normaal wurde droege en kalde om alle oerbliuwende focht en ûnrein te ferwiderjen om suvere Yttrium-metaal of ferbiningen te krijen.
Detectie-metoaden fan Yttrium
Common Detrection-metoaden befetsje foaral atoomsorkeringspektroskopy (AAS), induktyf koppeling plasma SPECTROMETRY (ICP-MS FULORESCECENS SPECORESCOPY (XRF), ensfh.
1. Atomyske opname spektroskopy (AAS):AAS is in faak brûkt foar kwantitative analyse-metoade geskikt foar it bepalen fan de Yttrium-ynhâld yn oplossing. Dizze metoade is basearre op de opname-ferskynsel as it doelelemint yn 'e stekproef it ljocht fan in spesifike golflingte absoreart. Earst wurdt it stekproef omboud ta in mjitbere foarm fia pretreatment stappen, lykas it droegjen fan gasstroffelen. Doe wurdt ljocht oerienkomt mei de golflingen fan it doelwinning yn 'e stekproef, wurdt de ljochtintensiteit troch it stekproef dat wurdt mjitten, en de Yttrium yn' e stekproef wurdt berekkene troch it fergelykje troch in standert Yttrium-oplossing fan bekende konsintraasje.
2 Induktyf koppele plasma massaspektrometry (icp-ms):Icp-ms is in heul gefoelige analytyske technyk geskikt foar it bepalen fan de Yttrium-ynhâld yn floeistof en bêst samples. Dizze metoade konverteart it stekproef yn opladen dieltsjes en brûkt dan in massale spektrometer foar massa-analyse. Icp-ms hat in breed detektyk berik en hege resolúsje, en kinne tagelyk de ynhâld fan meardere eleminten bepale. Foar de detectok fan Yttrium kin ICP-MS-limiten en hege krektens tige lege deteksje en hege krektens leverje.
3 race Fluorescence Spectrometry (XRF):XRF is in net-destruktive analytyske metoade geskikt foar de bepaling fan Yttrium-ynhâld yn solide en floeibere samples. Dizze metoade bepaalt de elemint tefreden troch it oerflak fan it oerflak fan 'e stekproef te bestridearjen en de karakteristike peak-yntinsiteit te mjitten fan' e fluorescens spektrum yn 'e stekproef. XRF hat de foardielen fan rappe snelheid, ienfâldige operaasje, en de mooglikheid om meardere eleminten tagelyk te bepalen. XRF kin lykwols ynterfereare wurde yn 'e analyze fan Yttrium, resultearje lykwols yn grutte flaters.
4. INduktyf koppele plasma optyske emission-útstjoeringsspektrometry (icp-oes):Inductively Coupled Plasma Optical Esmission Specission Spectrometry is in heul gefoelich en selektyf analytyske metoade dy't breed brûkt wurdt yn multyfelaasje analyse. It atomeart it stekproef en foarmet in plasma om de spesifike golflingte en yntensiteit o te mjittenF YttriumUtjefte yn 'e spektrometer. Neist de boppesteande metoaden binne d'r oare metoaden foar it elektryske metoade, ynklusyf elektryske metoade, ensfh. De seleksje fan in geskikte detaksjes, en kalibraasjekrêft binne faaks om de krektens te garandearjen om de krektens en betrouberens fan 'e mjittingsresultaten te garandearjen.
Spesifike tapassing fan Yttrium Adragyske opname-metoade
Yn elemintlike mjittingen, induktyf koppeling plasma massaspektrometry (icp-ms) is in heul gefoelich en multi-elemint analysetechnyk, dat wurdt faak brûkt om de konsintraasje fan eleminten te bepalen, ynklusyf Yttrium. It folgjende is in detaillearre proses foar it testen fan Yttrium yn ICP-MS:
1 Sample tarieding:
De stekproef moat meastentiids wurde ûntbûn of ferspraat yn in floeibere foarm foar analyse fan ICP-MS. Dit kin dien wurde troch gemyske ûntbining, wichtige metoaden fan 'e passende tariedingferwidering.
De tarieding fan 'e stekproef fereasket ekstreem skjinne omstannichheden om fersmoarging te foarkommen troch elke eksterne eleminten. It laboratoarium moat needsaaklike maatregels nimme om foarbyldbesmoarging te foarkommen.
2. Icp generaasje:
ICP wurdt generearre troch ynfiering fan argon of aron-soerstof mingde gas yn in sletten kwart PLASMA-fakkel. Induktyf mei hege frekwinsje produseart in yntinsive plasma-flam, dat is it útgongspunt fan 'e analyse.
De temperatuer fan it plasma is sawat 8000 oant 10000 graden Celsius, dy't heech genôch is om de eleminten yn it stekproef te konvertearjen yn ionyske steat.
3. Ionisaasje en skieding:Sadree't de stekproef it plasma ynkomt, wurde de eleminten yn it ionisearre. Dit betsjut dat de atomen ien of mear elektroanen ferlieze, foarmje opladen ionen. Icp-ms brûkt in massaspektrometer om de ionen fan ferskate eleminten te skieden, meastentiids troch massa-to-char-charge ferhâlding (m / z). Hjirmei kinne de ionen fan ferskate eleminten skieden wurde en letter analyseare.
4. MASS SPECTROMETRY:De skieden Ionen Fier in massaspektrometer yn, meast in fjouwerkant in fjouwerkante mass-spektrometer as in magnetyske scannen mass-spektrometer. Yn 'e massa spektrometer wurde de izeren fan ferskate eleminten skieden en ûntdutsen neffens har massa-to-char-ratio. Hjirmei kinne de oanwêzigens en konsintraasje fan elk elemint bepaald wurde. Ien fan 'e foardielen fan induktyf koppele plasma massaspektrometry is syn hege resolúsje, wêrtroch it meardere eleminten tagelyk kinne detektearje.
5. Gegevensferwurking:De gegevens generearre troch ICP-MS moatte meastentiids ferwurke wurde en analysearre om de konsintraasje fan 'e eleminten te bepalen yn' e stekproef. Dit omfettet it fergelykje fan it ferminderjen fan it ferminderjen fan it fermidden fan bekenden fan bekenden, en it útfieren fan kalibraasje en korreksje.
6 resultaatrapport:It lêste resultaat wurdt presintearre as de konsintraasje as massa-persintaazje fan it elemint. Dizze resultaten kinne brûkt wurde yn in ferskaat oan applikaasjes, ynklusyf ierde wittenskip, miljeuanalyze, iten testen, medysk ûndersyk, ensfh.
Icp-ms is in heul akkuraat en gefoelige technyk geskikt foar multi-elemint analyse, ynklusyf yttrium. It freget lykwols komplekse ynstrumintaasje en ekspertize, sadat it normaal wurdt útfierd yn in laboratoarium as in profesjonele analyse sintrum. Yn werklik wurk is it nedich om de passende metoade metoade te selektearjen neffens de spesifike behoeften fan 'e side. Dizze metoaden wurde breed brûkt yn 'e analyse en deteksje fan Ytterbium yn Laboratories en yndustry.
Nei it gearfangen fan boppesteande kinne wy konkludearje dat Yttrium in heul ynteressant is mei unike fysike en gemyske eigenskippen, wat is fan grutte betsjutting yn wittenskiplike ûndersyks- en applikaasjefjilden. Hoewol wy wat foarútgong hawwe makke yn ús begryp dêrfan, binne d'r noch in soad fragen dy't fierder ûndersyk nedich binne en ferkenning. Ik hoopje dat ús ynlieding kin helpe lêzers better te begripen dit fassinearjende elemint en ynspirearje elkenien syn leafde foar wittenskip en belangstelling foar ferkenning.
Foar mear ynformaasje Plskontakt mei ús opnimmeûnder:
Tel & Whats: 008613524231522
Email:Sales@shxlchem.com
Posttiid: NOV-28-2024